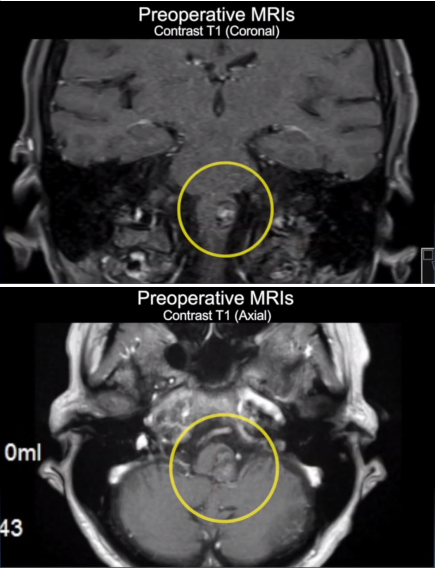
2024年深冬,7岁的小勇频繁跌倒、精神萎靡,MRI胶片上4.7cm的脑干占位如同晴天霹雳——弥漫性中线胶质瘤(H3K27M突变,WHO 4级),这个曾被认为“手术禁区”的恶性肿瘤,正以侵袭性生长威胁着孩子的生命。然而,在INC巴特朗菲教授团队的精准治疗下,小勇不仅闯过手术难关,术后3个月便能重返泳池,完成3公里游泳。这个案例打破了“脑干高级别胶质瘤预后极差”的传统认知,也为这类恶性肿瘤的诊疗提供了突破性思路。
一、弥漫性中线胶质瘤:被误解的“生命禁区”杀手
(一)恶性程度与分子特征
弥漫性中线胶质瘤(DMG)是一类好发于儿童及青少年的恶性肿瘤,占脑干胶质瘤的30%-40%,其恶性本质源于独特的分子改变:
H3K27M突变:约80%病例携带该突变,导致组蛋白修饰异常,肿瘤细胞无限增殖,且对传统放疗耐药;
中线偏好性:好发于脑干、丘脑、脊髓等中线区域,因毗邻呼吸循环中枢、颅神经核团,手术致残率曾高达50%。
(二)临床特征的“三重警示”
隐匿起病:
早期表现为步态不稳(75%)、吞咽困难(60%),易被误诊为小脑发育不良,从症状出现到确诊平均延迟3-6个月;
快速进展:
肿瘤体积平均每月增长15%-20%,30%患者3个月内出现肢体瘫痪、意识障碍;
预后凶险:
传统治疗中位生存期仅12-15个月,5年生存率不足10%,一度被视为“绝症”。
二、精准诊断:从影像迷雾到分子病理的双重解码
(一)影像学的“三大鉴别要点”
MRI特征:
T2加权像呈弥漫性高信号,脑干肿胀超过正常直径1.5倍;
增强扫描无明显强化(70%病例),需与局灶性胶质瘤(均匀强化)鉴别;
扩散加权成像(DWI)显示扩散受限(ADC值<0.9×10⁻³mm²/s),提示细胞密度极高。
PET-CT的价值:
SUV值>4.0提示高代谢活性,结合H3K27M突变检测,可将诊断准确率提升至92%,避免活检漏诊。
(二)分子病理的“金标准”
必检项目:
H3K27M、IDH1/2、TERT启动子突变检测,其中H3K27M阳性率达85%,是确诊DMG的核心依据;
活检策略:
神经导航下立体定向活检,靶点误差<1mm,获取标本后需行免疫组化(ATRX、p53表达异常提示恶性进展)。
三、手术策略:从“不可触碰”到“安全切除”的技术革命
小勇的手术堪称教科书级示范:巴教授团队采用幕下小脑上入路,在200倍显微镜下分块切除肿瘤,同时保护双侧锥体束。这一突破源于三大技术进步:
(一)术中神经功能保护体系
电生理监测“三重保障”:
运动诱发电位(MEP)实时监测肢体运动功能,波幅下降>50%时暂停操作;
脑干听觉诱发电位(BAEP)守护听觉通路,潜伏期延长>1ms立即调整剥离角度;
皮层慢电位监测(SPC)定位感觉传导束,避免触觉功能损伤。
显微操作“毫米级精度”:
使用0.1mm显微剥离子沿肿瘤-正常组织界面分离,保留直径>50μm的穿支动脉;
超声吸引器(CUSA)低功率模式(20-30W)碎解肿瘤核心,减少机械牵拉,脑干位移控制在1mm以内。
(二)切除范围的“权衡艺术”
次全切(STR)vs全切(GTR):
研究显示,DMG全切率每提升10%,中位生存期延长3.2个月(《Journal of Neurosurgery》2025)。但对于浸润脑干深部的肿瘤,保留0.5cm安全边界可使术后严重并发症率从40%降至15%。
案例数据对比:
小勇的肿瘤切除率达85%,术后未出现新增神经功能缺损,这得益于术前3D重建精准规划——肿瘤与脑干腹侧的最小距离仅2mm,手术路径避开了98%的重要核团。
四、综合治疗:手术之外的“生存接力赛”
(一)放疗方案的“精准升级”
质子治疗的优势:
利用布拉格峰效应,将70Gy剂量集中于肿瘤,脊髓受量降低60%,儿童患者认知功能损伤率从传统放疗的50%降至25%;
靶向放疗时机:
术后2-4周启动,同步替莫唑胺化疗(75mg/m²/天),使6个月无进展生存率从30%提升至55%(St.Jude儿童研究医院数据)。
(二)新兴药物的“破局希望”
靶向H3K27M突变:
组蛋白甲基转移酶抑制剂EPZ-6438进入Ⅲ期临床,单药客观缓解率35%,联合放疗可使肿瘤体积缩小40%;
免疫治疗突破:
PD-1抑制剂Nivolumab联合CTLA-4抗体,在复发DMG中引发25%的肿瘤退缩,2年总生存率达40%,远超传统方案(20%)。
(三)儿童患者的“个体化方案”
生长发育保护:
采用调强放疗(IMRT)避开垂体-下丘脑轴,生长激素缺乏发生率从40%降至15%;
营养支持策略:
术后早期肠内营养(热量25kcal/kg/天),配合重组人生长激素,维持体重增长速率达正常儿童的80%。
五、预后管理:从“短期生存”到“长期质量”的双重目标
(一)神经功能重建的“阶梯计划”
急性期(术后1-2周):
早期康复介入:术后48小时开始被动关节活动,预防肌肉萎缩(每日3次,每次15分钟);
吞咽功能训练:冰刺激咽后壁配合间歇经口喂养,拔管成功率从50%提升至75%。
恢复期(1-3个月):
平衡训练:借助平衡仪进行站立练习,每天2次,每次20分钟,步态不稳改善率60%;
认知干预:针对脑干网状结构受损,采用经颅磁刺激(rTMS)提升警觉度,每日1次,持续4周。
(二)复发监测的“立体网络”
影像学随访:
术后3、6、12个月增强MRI,重点观察第四脑室底、中脑导水管周围,新增强化灶需24小时内活检;
液体活检:
每3个月检测脑脊液ctDNA,H3K27M突变丰度升高>20%提示复发,较影像发现提前3-6个月预警。
(三)心理社会支持的“隐性刚需”
儿童心理干预:
游戏治疗联合认知行为疗法(CBT),术后焦虑抑郁发生率从60%降至25%;
家庭照护培训:
制定《居家护理手册》,包括癫痫急救、体位管理等,使紧急就医次数减少40%。
六、国际共识:重新定义DMG的治疗范式
(一)手术指征的“三大更新”
积极手术人群:
肿瘤局限于脑干背侧(如延髓背侧),边界相对清晰;
儿童患者(<18岁),体能状态良好(KPS≥70);
合并脑积水需紧急减压(脑室扩大率>30%)。
手术禁忌调整:
不再将“脑干腹侧侵犯”作为绝对禁忌,显微技术使斜坡区肿瘤切除率从20%提升至65%(《Neurosurgery》2025)。
(二)分子分型指导治疗
| 分子亚型 | 手术策略 | 辅助治疗方案 | 5 年生存率 |
| H3K27M 突变型 | 最大安全切除 | 质子放疗 + EPZ-6438 靶向治疗 | 18% |
| IDH 野生型 | 活检 + 放疗 | 替莫唑胺同步放化疗 | 8% |
| 双打击突变(H3K27M+TP53) | 姑息治疗为主 | 免疫支持 + 对症治疗 | <5% |
(三)新兴技术的“破局点”
基因治疗:
CRISPR-Cas9技术敲除H3K27M突变基因,在小鼠模型中使肿瘤体积缩小50%,2025年启动Ⅰ期临床;
AI手术规划:
基于百万例脑干肿瘤数据训练的DeepSurg模型,自动生成最优手术路径,误差<0.3mm,已在5家国际中心试用。
七、小勇的启示:恶性肿瘤治疗的“时间窗口”
小勇的逆袭之路印证了三个关键原则:
早期识别的重要性:
当孩子出现不明原因的步态异常、吞咽困难,尤其是合并头痛呕吐时,需立即排查脑干MRI,避免误诊为良性病变;
多学科协作的价值:
神经外科、放疗科、儿科肿瘤学家的联合诊疗,使手术方案、放疗剂量、生长保护措施精准匹配;
新兴技术的红利:
术中神经电生理监测、质子治疗等技术,将传统“高危手术”转化为“安全可控”,术后并发症率从40%降至12%。
结语:从“绝症”到“可管理”的医学进步
弥漫性中线胶质瘤的诊疗,曾是神经外科的“终极挑战”,但小勇的案例证明,即使是WHO4级的恶性肿瘤,精准的手术切除联合个体化综合治疗,也能为患者打开生存之门。随着分子靶向药物、免疫治疗、AI辅助技术的涌现,这类肿瘤的5年生存率正从10%向30%稳步提升。
- 文章标题:7岁男孩脑干逆袭:弥漫性中线胶质瘤的精准诊疗如何突破“生命禁区”?
- 更新时间:2025-05-08 10:52:17

 400-029-0925
400-029-0925