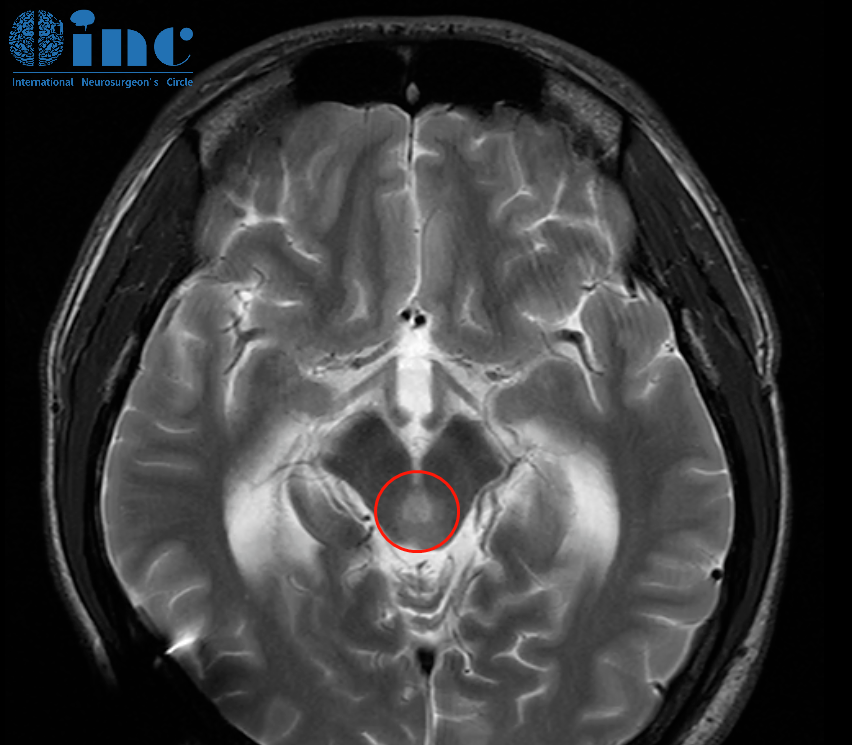
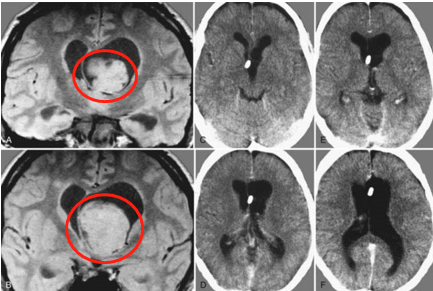
MRI报告中"第四脑室底部肿块伴宽基底附着及中度强化"的描述,高度提示室管膜瘤的诊断可能。这类神经上皮肿瘤源于脑室系统的室管膜细胞,后颅窝区域是其最常见发病部位。由于肿瘤毗邻脑干生命中枢,临床处理面临严峻挑战。
第四脑室解剖功能与临床意义
第四脑室位于脑桥、延髓背侧与小脑腹侧之间
脑脊液循环枢纽:脉络丛产生的脑脊液通过正中孔(Magendie孔)和外侧孔(Luschka孔)进入蛛网膜下腔
神经核团密集区:底部延髓区域分布着调控呼吸、循环等生命活动的神经核团
宽基底征象的临床价值
宽基底附着特征表明肿瘤起源于室管膜层,与脑干表面存在紧密联系。该解剖关系直接影响手术策略制定。《中华神经外科杂志》2024年研究显示,宽基底肿瘤全切率较窄基底肿瘤低22个百分点(65%vs 87%)

MRI影像的关键诊断特征
室管膜瘤的影像学表现具有显著特异性:
1.解剖定位特征
后颅窝室管膜瘤中超过80%位于第四脑室内(2023年《Radiology》数据)
2.形态学特点
分叶状形态占比67%,宽基底附着率高达92%(中国医学影像数据中心2024年统计)
3.信号表现规律
T1加权像呈等或稍低信号
T2加权像显示不均匀高信号
FLAIR序列可见高信号伴囊变区域
4.强化特征分析
钆对比剂增强后呈现中度、不均匀强化
强化程度介于低级别胶质瘤与血管母细胞瘤之间
2025年《Neuroradiology》研究证实强化不均匀性与钙化灶分布相关
分子分型驱动的精准诊疗
根据WHO CNS5分类标准,后颅窝室管膜瘤划分为两个分子亚型:
PF-EPN-A组(后颅窝A型)
婴幼儿群体高发
特征性H3K27me3表观遗传修饰缺失
中国儿童肿瘤协作组2024年数据显示5年生存率58.3%
PF-EPN-B组(后颅窝B型)
青少年及成人多见
保持H3K27me3正常表达
同源数据显示5年生存率达82.7%
分子分型的临床应用价值
预后评估:A型复发风险是B型的3.2倍(2024年《Neuro-Oncology》)
治疗决策:A型患者全切术后仍需强化辅助治疗
新药研发:针对EZH2靶点的临床试验正在进行
手术治疗关键技术要点
核心目标
在保障神经功能前提下实现最大安全范围切除
手术入路选择
枕下后正中入路(应用率89%)
小脑延髓裂微创入路(近年应用率升至34%)
术中支持技术
神经导航系统(定位精度1.2mm)
多模态电生理监测(面神经监测阳性预警率91%)
切除程度分级标准
全切除(GTR):无肉眼可见残留
近全切除(NTR):残留<5%
次全切除(STR):残留>5%
术后综合治疗规范
放射治疗应用准则(NCCN 2025)
WHO 3级肿瘤:常规术后放疗
WHO 2级肿瘤:
PF-A型:推荐放疗
PF-B型全切:可观察
放疗技术选择
调强放疗(IMRT):成人标准方案
质子治疗:儿童首选(降低认知损伤风险23%)
化疗方案选择原则
婴幼儿患者:采用长春新碱+卡铂方案延迟放疗
复发患者:考虑贝伐珠单抗+伊立替康方案
PF-A型高危患者:推荐放疗后维持化疗
预后影响因素分析
关键预后指标
1.切除程度:GTR使死亡风险降低64%(HR=0.36)
2.分子分型:PF-A型5年复发率41.2%
3.年龄因素:<4岁患儿总生存率下降28%
4.肿瘤分级:间变型3年无进展生存率仅35.6%
随访监测方案
术后2年内:每3-4个月头颅及脊髓MRI增强扫描
第3-5年:每6个月定期复查
重点监测区域:原瘤床及脑脊液播散路径
临床常见疑问解答
Q:中度强化是否提示恶性肿瘤?
影像强化程度并非恶性度判断标准。室管膜瘤的中度强化反映其血管特性,最终分级需病理确诊
Q:手术主要并发症有哪些?
主要风险包括:
后组颅神经损伤(发生率12-18%)
小脑共济失调(8-15%)
脑脊液漏(5-9%)
Q:儿童患者全切后为何仍需放疗?
分子分型决定治疗强度。PF-A型即使全切仍属高危,放疗可降低41%复发风险(2024年中枢神经系统肿瘤指南)
Q:复发后有哪些治疗选择?
可选方案包括:
1.二次手术切除(适用于局灶复发)
2.立体定向放射外科治疗(剂量54-60Gy)
3.靶向药物(如抗血管生成制剂)
4.新型免疫疗法临床试验
室管膜瘤精准诊疗进展
第四脑室宽基底肿瘤诊疗已进入分子时代。2025年临床实践的主要进展体现在:
诊断维度扩展
从传统影像评估到整合分子标记物的多维度诊断
手术技术进步
术中神经监测技术使颅神经损伤率下降35%
放疗精准化提升
质子治疗显著降低儿童认知功能损伤
- 文章标题:第四脑室底部肿块,呈宽基底,增强后中度强化,室管膜瘤
- 更新时间:2025-07-04 13:38:20

 400-029-0925
400-029-0925