脑膜瘤是颅内最常见的原发性肿瘤之一,占所有脑肿瘤的30%左右。这种起源于脑膜(包裹大脑和脊髓的保护膜)的病变,绝大多数属于良性,生长速度缓慢。2024年《柳叶刀神经学》的研究数据显示,全球脑膜瘤年发病率约为8.35/10万(95%CI:7.92-8.78)。值得注意的是,女性发病率是男性的2-3倍,45岁左右是发病高峰。虽然多数生长缓慢,但不同病理类型的临床管理策略差异显著呢。相关阅读:脑膜瘤治疗:原则、费用、最佳治疗方法、几种治疗方案方法
病理分级与生物学特征
WHO分级体系
世界卫生组织(WHO)将脑膜瘤分为三级:
- Ⅰ级(良性):占比约80%,细胞分化良好,年生长速度通常小于2毫米
- Ⅱ级(非典型):占15%,有丝分裂象增多(4-19个/10HPF)
- Ⅲ级(间变性/恶性):仅占5%,侵袭性强,可发生远处转移
Ⅰ级患者5年生存率超过92%,而Ⅲ级骤降至37.7%(P<0.01)。这种生存差异与肿瘤的分子特征密切相关,比如NF2基因突变在非典型脑膜瘤中检出率高达60%呢。

临床表现与症状演进
隐匿期特征
早期可能完全没有症状,尤其当肿瘤位于非功能区时。随着体积增大,常见表现包括:
- 慢性头痛(70%患者首发症状)
- 偶发癫痫(年发作1-2次)
- 单侧肢体麻木或无力
进展期警示信号
当出现这些变化需高度警惕:
- 头痛频率从每月几次发展为每天持续疼痛
- 视力在3个月内下降超过50%
- 性格突变(如温和者变得暴躁易怒)
- 癫痫发作频率骤增
2024年《神经肿瘤学杂志》研究指出:症状进展速度与病理分级显著相关,恶性脑膜瘤症状恶化速度是良性的5-8倍。
精准诊断技术
影像学核心方法
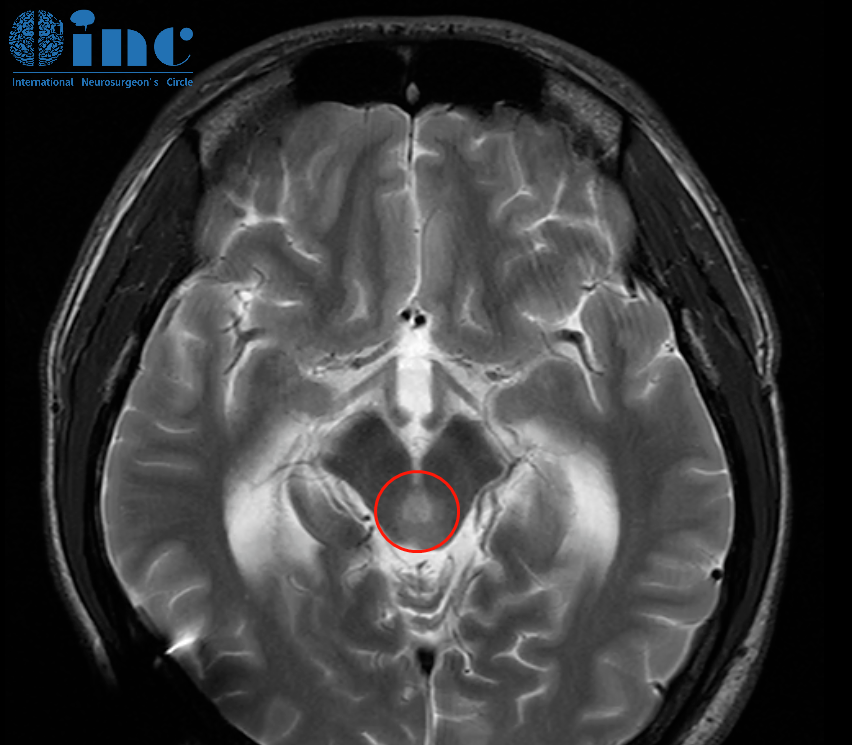
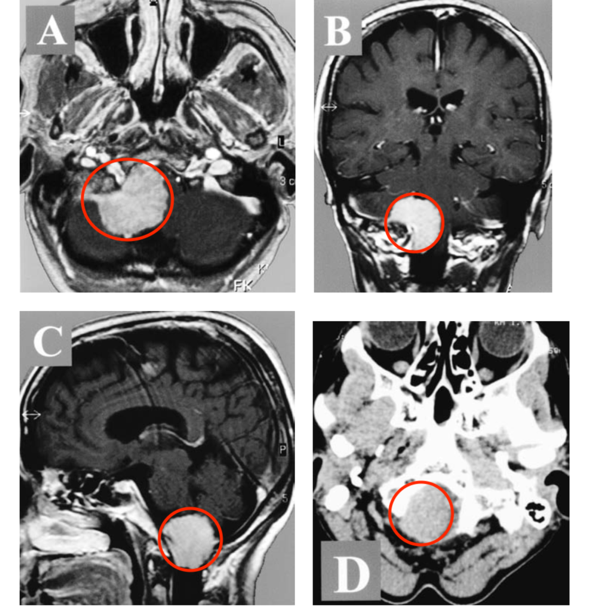
- MRI平扫+增强:诊断金标准,可显示"脑膜尾征"(肿瘤基底硬膜强化)
- CT扫描:辅助评估颅骨改变(40%伴骨质增生)
- PET-CT:SUV值>3.0提示恶性可能(敏感度82.3%)
病理确诊要点
术后必须进行:
1.组织学分型(9种良性亚型)
2.有丝分裂计数
3.免疫组化检测(Ki-67指数>5%提示高复发风险)
《NCCN中枢神经系统肿瘤指南(2025版)》强调:对于颅底或功能区肿瘤,应加做DTI纤维束成像,以降低手术致残风险。
分层治疗策略
观察等待原则
适用于:
- 无症状Ⅰ级肿瘤
- 直径<3cm
- 高龄或合并严重基础疾病者
复查方案:首年每6个月MRI,稳定后改为年度随访
手术治疗关键点
全切除(Simpson I级切除)是治愈基石:
- 凸面脑膜瘤全切率达90%
- 颅底肿瘤全切率约60-70%
术中技术包括:
- 神经导航(定位误差<1mm)
- 神经电生理监测
- 荧光引导切除
放射治疗新进展
- 立体定向放疗(SRS):适用于<3cm残留灶(控制率85%)
- 质子治疗:减少海马区受量(保护认知功能)
- 分割放疗(54Gy/30f):用于Ⅱ-Ⅲ级术后辅助
预后与长期管理
复发风险矩阵
| 影响因素 | 低风险组 | 高风险组 |
| 切除程度 | Simpson I-II级 | Simpson IV-V级 |
| 病理分级 | WHO I级 | WHO III级 |
| Ki-67指数 | <5% | >10% |
随访监测方案
- 术后第1年:每3-6个月MRI
- 术后2-3年:每6个月复查
- 3年以上:每年评估
重点监测:新发强化灶、ADC值降低、rCBV升高
迟发并发症防控
- 认知障碍:放疗后MoCA评分下降>3分需干预
- 内分泌紊乱:每年检测垂体激素谱
- 放射坏死:灌注MRI显示rCBV<0.6
热点问题解答
Q:体检发现脑膜瘤必须手术吗?
不一定呢!对于无症状的Ⅰ级小肿瘤(<3cm),首选定期观察。2025版NCCN指南明确:这类患者立即手术的获益并不优于密切随访。
Q:脑膜瘤会遗传给子女吗?
绝大多数是散发病例。但Ⅱ型神经纤维瘤病患者子女的发病风险增加7-10倍(《Nature Genetics》2024),建议高危人群40岁起定期筛查。
Q:伽玛刀能替代开颅手术吗?
对于<3cm的颅底肿瘤,立体定向放疗可作为手术替代方案。但直径>4cm或压迫脑干的肿瘤,仍首选手术减压。
Q:术后为什么还要做放疗?
当病理报告显示WHO II-III级,或切除不彻底时,术后放疗能降低复发风险达40%(2025 CNS年会数据)。不过Ⅰ级全切患者通常不需要哦。
Q:复发有哪些征兆?
警惕这些信号:头痛模式改变、癫痫复发、新发神经缺损症状。建议及时复查MRI增强扫描,重点关注原手术残腔边缘。
- 文章标题:脑膜瘤从病理分级到精准治疗
- 更新时间:2025-07-05 09:48:23

 400-029-0925
400-029-0925