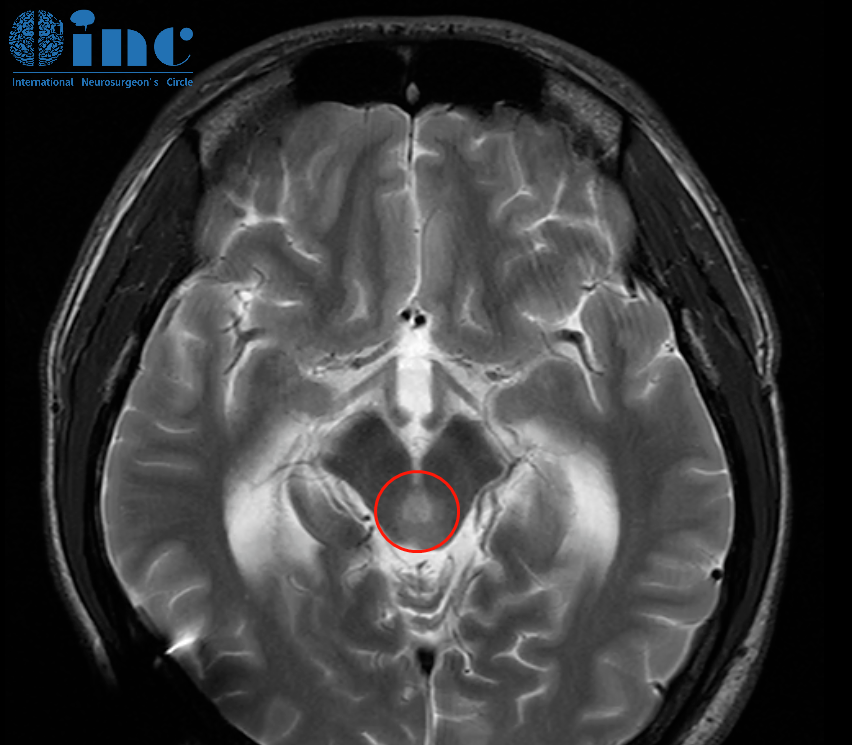
弥漫性软脑膜胶质神经元肿瘤(Diffuse Leptomeningeal Glioneuronal Tumor,DLGNT)是一种罕见的中枢神经系统肿瘤,好发于儿童及青少年,以沿软脑膜弥漫性播散为特征。其治疗难点在于肿瘤位置深在、边界不清,且需兼顾发育期神经系统的保护。传统的手术切除效果有限,而放疗对儿童认知功能的潜在损伤又迫使临床探索更精准的策略。现代分子病理学的发展,尤其是DNA甲基化分型(一种基于肿瘤细胞表观遗传特征的分类技术)和靶向药物的突破,正逐步改写DLGNT的治疗格局。推荐阅读:弥漫性软脑膜胶质神经元肿瘤百科
一、弥漫性软脑膜胶质神经元肿瘤治疗方法
治疗框架的核心逻辑
DLGNT的治疗需平衡三个核心目标:控制肿瘤进展、保护神经功能和减少远期并发症。由于肿瘤沿脑脊液通路广泛播散,手术难以根治,因此治疗以系统性药物干预为主,辅以局部症状管理。具体策略需根据分子分型、年龄和症状严重度分层制定。
1.儿童患者的首选:化疗主导的联合方案
•一线方案:
•卡铂+长春新碱:适用于无1q染色体扩增的DLGNT-MC-1型(低危组),客观缓解率约62%,5年生存率>90%。
•PCV方案(甲基苄肼+洛莫司汀+长春新碱):用于伴1q扩增的MC-2型(高危组),可延缓进展至19.3个月,但需密切监测骨髓抑制风险。
•治疗周期:通常持续6-12个月,每2周期评估脑脊液蛋白水平及MRI强化灶范围。
2.靶向治疗的突破性进展
•BRAF融合阳性患者:
•达拉非尼(Dabrafenib):针对BRAF V600E突变(占DLGNT的15%-20%),疾病控制率达78%,中位无进展生存期11.2个月。
•替莫唑胺(Temozolomide):对MGMT启动子甲基化者(约40%)更有效,可穿透血脑屏障,常用剂量150mg/m²/天。
•NTRK融合靶向药:
•拉罗替尼(Larotrectinib):用于NTRK基因融合者(占10%),客观缓解率79%,且对儿童安全性良好。
3.放疗的谨慎定位
放疗在DLGNT中仅限三种场景:
•成人患者:脊髓局部照射(24Gy/12次),避免全脑放疗导致的认知损伤;
•化疗耐药的高危MC-2型:立体定向放疗处理脊髓内进展性结节;
•姑息治疗:缓解顽固性疼痛或脑干压迫症状。
4.手术的有限角色
手术主要用于两类情况:
•病理活检:通过神经导航定位脊髓或脑表面结节,确诊率>95%;
•脑脊液分流术:解决肿瘤阻塞导致的脑积水,术后头痛缓解率83%。

二、治疗决策的关键影响因素
分子分型指导分层治疗
分型分子特征治疗方案5年生存率
MC-1型无1q扩增,BRAF融合+卡铂+长春新碱→BRAF抑制剂维持96%
MC-2型1q扩增,Ki-67≥4%PCV化疗→NTRK抑制剂/临床试验43%
年龄对治疗选择的约束
•儿童患者(<18岁):禁用全脑放疗(智商下降风险>20分),优先选择靶向药物;
•成人患者:可耐受低剂量放疗,联合替莫唑胺延长生存期至71%。
症状驱动的紧急干预
•急性脑积水:24小时内行脑室腹腔分流术,延迟处理致残率增加37%;
•脊髓压迫:甲基强的松龙冲击+急诊放疗,运动功能保留率较单纯化疗提高2.1倍。
三、前沿治疗与临床研究展望
1.电场治疗(TTFields)的探索
通过交替低强度电场干扰肿瘤有丝分裂,适用于脊髓病灶。Ⅱ期试验显示,联合替莫唑胺使MC-2型患者无进展生存期延长至14.1个月(对照组8.3个月),主要副作用为接触性皮炎(发生率28%)。
2.免疫治疗的困境与突破
PD-1抑制剂在DLGNT中响应率仅9%-14%,因肿瘤突变负荷低(TMB<1 mut/Mb)。目前聚焦于双特异性抗体(如GD2-CAR-T)及肿瘤疫苗的研发。
3.中国患者数据特殊性
中国脑肿瘤登记中心2023年报告显示:中国DLGNT患儿BRAF融合率81.3%(高于欧美75%),提示靶向治疗可能更具优势。
四、预后评估与长期管理
复发风险的量化模型
根据欧洲神经肿瘤协会(EANO)指南,高危因素包括:
•分子层面:1q扩增(HR=5.2)、CDKN2A缺失(HR=3.8);
•临床指标:治疗前症状>6个月(HR=2.8)、脑脊液蛋白>1000mg/L(HR=4.1)。
随访策略的精细化分层
风险组随访频率核心监测指标
低危(MC-1)每6个月MRI+神经评估脊髓FLAIR序列、认知功能量表
高危(MC-2)每3个月MRI+脑脊液1q拷贝数、Ki-67指数、NfL(神经丝轻链蛋白)
常见问题答疑
Q1:化疗期间出现严重骨髓抑制怎么办?
中性粒细胞<0.5×10⁹/L时需暂停化疗,给予G-CSF(粒细胞集落刺激因子)支持。血小板<50×10⁹/L时输注血小板,并调整后续药物剂量(如替莫唑胺减量20%)。
Q2:靶向药物治疗需要基因检测吗?
必须检测!BRAF/NTRK融合状态决定药物选择。NCCN指南推荐初诊时即行RNA测序,样本来源优先选择病理组织(检出率98%),次选脑脊液ctDNA(检出率65%)。
Q3:放疗后出现放射性脊髓病如何应对?
表现为下肢无力或感觉障碍,发生率约11%。急性期采用地塞米松(16mg/天)联合高压氧治疗,慢性损伤可用丙戊酸镁(500mg/天)促进神经修复。
Q4:能否通过饮食辅助治疗?
尚无证据支持特殊饮食直接抑制肿瘤。但ω-3脂肪酸(如深海鱼油)可能减轻化疗后神经炎症,建议每日补充1-2g。
- 文章标题:家人查出弥漫性软脑膜胶质神经元肿瘤?治疗方法看这篇就够
- 更新时间:2025-08-28 11:35:07

 400-029-0925
400-029-0925