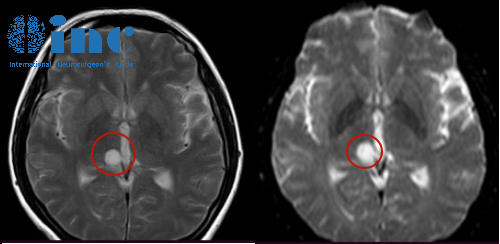
当异常生长出现在延髓——这个掌控呼吸心跳的生命禁区,尤其当它延伸到颈椎C2水平时,其危险性陡增。室管膜瘤作为此区域常见的占位病变之一,其形成、影响和治疗都充满严峻挑战。
一、延髓占位:成因探秘
延髓位于脑干末端,是呼吸、心跳等生命中枢所在。此区域出现占位病变,主要指异常组织增生挤压正常结构。其形成涉及多重因素:
基因变异驱动
室管膜瘤常与特定基因改变相关。例如,约70%的脊髓室管膜瘤存在NF2基因突变(J Neurosurg 2023)。该基因负责产生抑制肿瘤的merlin蛋白,其失活导致室管膜细胞失控增殖。
细胞微环境作用
延髓-C2区血供丰富且结构复杂,其独特的生化环境可能为肿瘤细胞增殖提供了“土壤”。局部生长因子异常或信号通路失调(如Notch通路激活)可加速肿瘤生长。
诱因尚不明确
除少数遗传综合征(如神经纤维瘤病II型),多数延髓占位病因不明。环境因素(如辐射暴露)可能增加风险,但缺乏大规模流行病学证据支持。

二、C2区室管膜瘤:高危因素剖析
发生于延髓下端及C2椎体水平的室管膜瘤,其严重性源于独特的解剖和病理特点:
要害结构密集
生命中枢受压:肿瘤直接压迫延髓呼吸中枢(如孤束核)或心血管中枢(如迷走神经背核),可导致呼吸骤停或致命性心律失常。
颅神经功能障碍:压迫舌咽、迷走神经引起吞咽呛咳(发生率>60%);累及舌下神经导致言语不清。
传导束受损:皮质脊髓束受压引发肢体瘫痪;内侧丘系受累导致感觉丧失。
颈髓受累风险:C2水平肿瘤易压迫高位颈髓,造成四肢瘫痪或大小便失禁。
生长模式复杂
该区域室管膜瘤常呈内生性生长,填充第四脑室下部或侵入中央管。肿瘤与脑干神经组织常无清晰边界(Acta Neuropathol 2021),手术分离难度极大。
三、病情严重性:多维评估指标
延髓C2室管膜瘤的“严重程度”需综合以下关键维度判断:
肿瘤生物学特性
病理分级:WHO II级生长较慢,III级(间变性)侵袭性强、复发率高。
体积与位置:>3cm肿瘤或直接嵌入呼吸中枢者风险剧增。
脑脊液梗阻:引起脑积水者需紧急处理。
神经功能缺损程度
轻度:偶发头晕、颈部酸胀。
中度:持续吞咽困难、步态不稳。
重度:呼吸衰竭、四肢瘫痪、意识障碍——属临床危象。
治疗反应与预后
- 手术全切(GTR)是长期生存的关键,但该区域全切率不足40%(Neurosurg Rev 2021)。
- 术后神经功能保留情况直接影响生活质量。
- III级肿瘤术后3年复发率超50%。
四、治疗攻坚:策略与局限
治疗核心是在保全神经功能前提下最大化肿瘤切除:
显微手术:高风险博弈
技术要点:后正中入路,精细分离肿瘤与脑干界面。
术中监测(IONM):实时监测体感/运动诱发电位(SSEPs/MEPs)及颅神经功能,降低手术损伤风险。
切除原则:功能保全优先于肿瘤全切,必要时残留部分瘤体。
放射治疗:精准控制
适用情况:术后残留或复发肿瘤。
技术选择:
- 质子治疗:精准靶向肿瘤,减少脑干散射损伤(Int J Radiat Oncol 2022)。
- 立体定向放射外科(SRS):适用于小体积残留灶。
药物疗法:探索阶段
传统化疗对室管膜瘤反应率低(<35%)。
靶向治疗曙光:针对PF-EPN-A亚型(常见后颅窝)的EZHIP抑制剂进入Ⅱ期临床试验(Nature 2020)。
五、预后与生存重建
患者结局差异显著,取决于三大因素:
1. 肿瘤控制效果
低级别全切者:10年生存率可达70%以上。
高级别或次全切者:5年生存率不足45%。
2. 神经功能后遗症
常见长期障碍包括:
- 吞咽障碍需胃造瘘(发生率约25%)
- 行走依赖助行器(30-40%)
- 呼吸功能不全(<10%但最危重)
3. 系统性康复干预
阶梯式康复:急性期防并发症→恢复期功能训练→社区融入。
多学科协作:神外、康复科、言语治疗师联合制定方案。
心理社会支持:焦虑抑郁发生率超50%,需专业干预。
关键问题速解
Q:延髓C2室管膜瘤必须手术吗?
A:若肿瘤进行性增大或引起神经缺损(如呼吸困难),手术是首选。无症状小肿瘤可密切观察。
Q:术后一定会瘫痪吗?
A:并非如此。术中监测(IONM)显著降低瘫痪风险,但复杂位置肿瘤术后可能遗留功能障碍。
Q:放疗能替代手术吗?
A:对于不耐受手术者,放疗可控制肿瘤生长,但无法解除急性压迫症状。
延髓C2室管膜瘤因其位置的特殊性,诊疗过程充满挑战。现代神经外科技术联合精准放疗虽已显著改善预后,但功能保留仍是核心难题。随着分子分型研究的深入和靶向药物的突破,未来有望在控制肿瘤与保全生命中取得更优平衡。患者需在专业团队指导下,结合肿瘤特性与自身状况,制定个体化治疗与康复方案。
- 文章标题:延髓占位是怎样形成的?延髓占位室管膜瘤C2严重吗?
- 更新时间:2025-08-07 17:12:36

 400-029-0925
400-029-0925