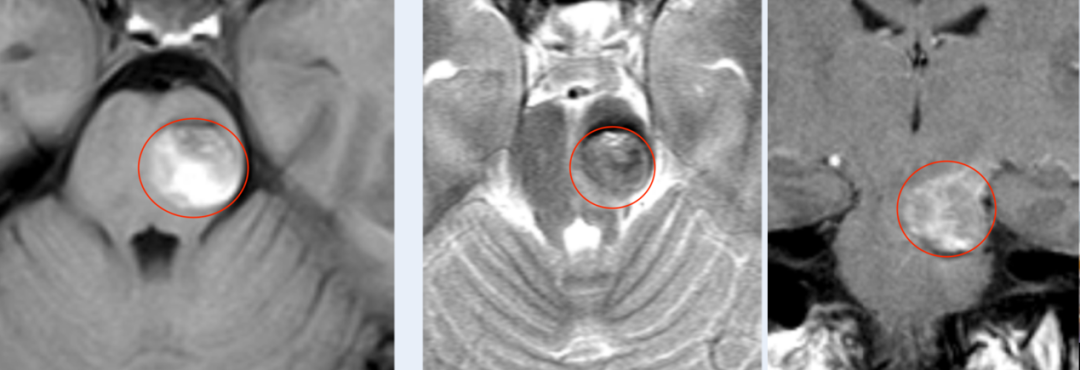
大脑半球及小脑半球脑白质T2信号增高,是指在磁共振成像(MRI)T2加权像上,脑白质区域出现异常的高信号影。这一影像学表现提示局部组织含水量增加或髓鞘结构发生变化,常见于多种神经系统疾病或年龄相关的退行性改变。发现此类信号改变后,关键不在于恐慌,而在于弄清楚它背后的原因。
T2信号增高是怎样形成的
T2加权成像通过检测组织中水分子的弛豫特性来形成对比。正常脑白质含水量约为70%,髓鞘包裹的轴突束呈现相对低信号。当白质区域T2信号异常增高时,通常意味着该处自由水含量上升或组织结构变得松散。临床数据显示,在40岁以上人群中,MRI检出脑白质T2高信号的比率约为50%至60%,且随年龄增长持续上升。这一比例说明了两个事实:它非常常见;它不等同于疾病。
从病理学角度分析,信号增高的机制主要有三类。第一类是脱髓鞘改变,即髓鞘层结构完整性受损,导致水分子在髓鞘间隙中积聚,常见于多发性硬化等免疫相关疾病。第二类是缺血性改变,脑白质由穿支动脉供血,对低灌注极为敏感,长期慢性缺血可导致白质疏松和T2信号升高,这一机制在脑小血管病中最为常见。第三类是代谢或中毒性改变,如一氧化碳中毒后迟发性脑病、维生素B12缺乏等,也可表现为白质T2高信号。不同机制的预后差异极大,区分清楚是首要步骤。
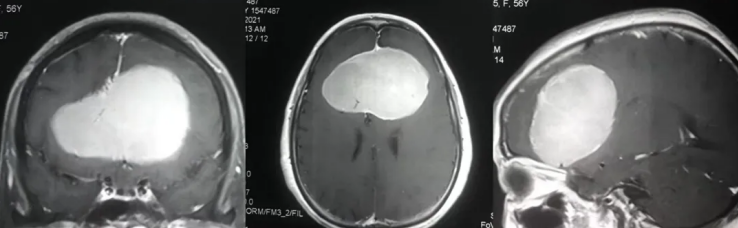
最常见的原因是什么
临床实践中,大脑半球及小脑半球脑白质T2信号增高最常见的根本原因是脑小血管病。这类疾病占所有卒中病因的20%至25%,而白质高信号是脑小血管病在MRI上最典型的表现之一。其发病基础是脑内小动脉管壁增厚、管腔狭窄,导致白质区域慢性低灌注。长期的高血压是最明确的危险因素,糖尿病、吸烟、高脂血症等代谢综合征相关因素也显著加速其进展。
小脑半球的白质T2信号增高相对大脑半球少见,但并非无临床意义。小脑位于后颅窝,血液供应主要来自椎-基底动脉系统的小分支。当这些穿支血管发生病变时,小脑白质同样可以出现缺血性改变。在55岁以上人群中,脑白质高信号的总患病率约为87%,但累及小脑的比例远低于大脑,通常只占其中的10%至15%。如果报告同时提到大脑和小脑半球均有改变,医生通常会将其视为全身性小血管病变的一部分,而非局部单独疾病。
信号增高代表多严重的病情
这是所有患者最关心的问题,也是医生最需要谨慎回答的问题。从临床经验来看,T2信号增高的严重程度需要结合三个维度来判断,而不是单独看影像报告。这三个维度分别是:信号分布的范围、是否累及关键功能区、以及是否有相应的临床症状。
关于范围评估,临床广泛使用Fazekas分级系统。0级代表无可见改变;1级(斑点状)指信号点直径小于3毫米,数量通常少于10个;2级(早期融合)指信号开始融合成片,但尚未广泛分布;3级(广泛融合)指大范围融合性高信号,通常双侧对称分布。研究数据表明,Fazekas 1-2级在60岁以上人群中属于相对良性发现,进展速度通常很慢;而3级患者在5年内发展为认知功能减退的风险约为30%至40%,需更积极的危险因素控制。
关于功能区评估,如果T2高信号累及胼胝体(连接两侧大脑半球的最大的白质束)、内囊(运动和感觉纤维的密集通道)或小脑中脚(连接小脑与大脑皮层的关键桥梁),其临床意义通常大于单纯累及脑室周围或皮质下散在区域。因此,拿到MRI报告后应请神经内科医生结合具体分布位置进行个体化解读,而非自行通过网络信息进行归类。
需要做哪些进一步检查
发现白质T2信号增高后,下一步检查并非越多越好。过度检查不仅浪费医疗资源,还可能增加患者的心理负担。合理的检查策略应遵循"分层递进"原则,先明确最常见原因,再排查需要特殊干预的疾病。
第一层检查针对最常见的危险因素,包括血压(需测量卧位和立位血压以排除体位性低血压)、空腹血糖、糖化血红蛋白、血脂四项(同型半胱氨酸和脂蛋白a应作为可选补充)、颈动脉超声(评估全身动脉粥样硬化程度)。这些检查价格低廉,覆盖了约80%以上的潜在病因。第二层检查根据第一层结果个体化选择,如果患者年龄较轻(小于55岁)且无明显血管危险因素,应考虑排查多发性硬化(可行视神经MRI、脑脊液寡克隆带检测)、自身免疫性脑炎或遗传性脑白质病(如肾上腺脑白质营养不良基因筛查)。第三层检查针对特定临床线索,如有步态异常或尿失禁表现,需评估正常压力脑积水的可能;如伴认知功能快速下降,需排查感染、代谢或中毒性病因。
日常生活应该如何管理
影像改变一旦发生,目前尚无药物能够完全逆转已形成的白质损伤。但这并不意味着无所作为——相反,这是为数不多的"通过控制进程来改变预后"的疾病窗口。大量循证医学证据表明,系统性的危险因素管理可以显著延缓白质病变的进一步进展。
血压管理是最有效的单一干预措施。建议将收缩压控制在130毫米汞柱以下(老年人可根据耐受性适当放宽至140毫米汞柱),目标舒张压不超过80毫米汞柱。收缩压每降低5毫米汞柱,脑卒中风险减少约12%,白质病变进展速度同步减缓。糖尿病患者应将糖化血红蛋白控制在7%以下,但老年患者需警惕低血糖风险,空腹血糖控制在6至8毫摩尔每升区间通常是合理的。
生活方式干预中,有氧运动是最强有力的证据支持。每周进行150分钟中等强度有氧运动(如快走、游泳、骑行),可将认知功能下降风险降低约35%。地中海饮食模式(富含橄榄油、深海鱼类、蔬菜和坚果)同样有研究支持其对脑小血管健康的保护作用。戒烟是最快速有效的措施——戒烟后24小时内血液中的一氧化碳水平即可恢复正常,血管内皮功能在数周内开始改善。此外,建议保持充足的睡眠(每晚7至8小时),睡眠呼吸暂停综合征患者应积极接受持续正压通气(CPAP)治疗,因为睡眠缺氧会显著加速白质病变进展。
你可能还想知道的几件事
高信号会消失吗?大多数情况下,已形成的白质T2高信号不会完全消失。脱髓鞘疾病(如多发性硬化)在治疗有效时,水肿消退可使信号部分恢复,但已坏死的髓鞘无法再生。血管源性改变(脑小血管病)属于慢性结构性损伤,理论上不可逆,但这并不意味着症状必然加重——关键在于控制危险因素,阻止新的损伤出现。
报告中的"脱髓鞘"和"缺血性改变"有何不同?两者在MRI上均可表现为T2高信号,但含义不同。脱髓鞘通常指髓鞘这个"绝缘层"受损,而轴突本身可能保持完整,治疗前景相对较好;缺血性改变指整个组织因血液供应不足而受损,轴突和髓鞘均受累。医生通常会结合发病年龄、病程特点及其他序列(如DWI、T1加权)综合判断,必要时建议进一步检查以明确性质。
和老年痴呆有什么关系?严重的白质T2高信号(尤其是Fazekas 3级)与血管性认知障碍密切相关。白质病变破坏了不同脑区之间的神经连接,导致信息传递效率下降,表现为注意力不集中、反应速度变慢、执行功能减退等。流行病学数据显示,脑白质高信号患者未来发生痴呆的风险是正常人群的2至3倍,但这一风险主要来自未良好控制的血管危险因素,而非影像学改变本身。
需要多久复查一次MRI?如果首次发现时信号范围较小(Fazekas 1-2级)且无明显临床症状,建议2至3年后复查,以评估进展速度。如果信号范围较大( Fazekas 3级)、已知存在高血压或糖尿病等危险因素、或已有认知功能改变,建议1至2年复查。复查的主要目的不是"看高信号有没有变小",而是评估病变范围是否扩大、新发梗死灶是否出现——这才是真正影响预后的指标。
有药物可以治疗吗?目前尚无专门批准用于逆转脑白质T2高信号的药物。临床常用的一些药物(如尼莫地平、银杏叶提取物、胞磷胆碱等)有一定理论基础,但循证证据强度有限,不建议作为主要治疗手段。优先选择仍是危险因素控制。如果同时存在明确的多发性硬化等免疫性疾病,则应接受相应的免疫调节治疗,这属于完全不同的治疗路径,需另案处理。
发现脑白质T2信号增高,本质上是一次健康预警。它的价值不在于影像本身,而在于提醒我们:脑血管系统正在经历某种程度的变化。冷静应对、系统评估、积极控制危险因素,是将这一预警信号转化为健康管理机会的最优路径。别急着下结论——找专业医生、读懂自己的报告、把能控制的因素控制住,这才是最应该做的事。
- 文章标题:大脑小脑半球脑白质T2信号增高意味着什么?别急着下结论
- 更新时间:2026-05-13 10:11:56

 400-029-0925
400-029-0925