少突胶质细胞瘤作为胶质瘤的重要亚型,其病理诊断不仅依赖传统组织学特征,更需整合分子标志物与影像关联性分析。这类肿瘤占胶质瘤的5%-10%,高峰发病年龄在40-60岁,男性略多于女性(比例约1.21:1)。其独特的钙化倾向(CT检出率70%-90%)和1p/19q染色体联合缺失(发生率>80%)构成了诊断的双支柱。随着WHO中枢神经系统肿瘤分类标准的更新,病理诊断已从单纯的细胞形态观察,进阶为结合分子分层的整合模式。
病理分级与分类演变
少突胶质细胞瘤的分级遵循WHO四级系统,但实际仅涉及Ⅱ级(低级别)和Ⅲ级(间变性),不存在Ⅰ级和Ⅳ级类型——后者被归类为胶质母细胞瘤。
分级核心标准
•WHOⅡ级:
•细胞特征:肿瘤细胞密度中等,核呈圆形或卵圆形,核周空晕形成典型“煎蛋样”外观;核分裂象罕见(<2个/10高倍视野)。
•分子要求:必须存在1p/19q共缺失,否则需重新分类为星形细胞瘤。
•WHOⅢ级(间变性):
•恶性转化标志:细胞密度显著增高,核异型性明显,核分裂象≥4个/10高倍视野;微血管增生或坏死虽非必需,但若出现需警惕胶质母细胞瘤可能。
分级误区警示:
•无纯Ⅳ级少突胶质细胞瘤:若出现假栅栏状坏死或微血管团簇状增生,应诊断为IDH突变型胶质母细胞瘤。
•混合性胶质瘤的特殊性:少突星形细胞瘤需同时检测IDH突变和1p/19q状态,若仅后者阳性则归为纯少突型。
组织病理学特征
大体与显微结构
•大体标本:肿瘤边界相对清晰(但非真包膜),切面灰红色,质地柔韧;钙化区域触之砂砾感,囊变罕见。
•特征性构型:
•蜂窝状结构:石蜡切片中肿瘤细胞胞质肿胀透亮,核居中,形似蜂巢(甲醛固定后人工假象)。
•分支状血管:薄壁血管分支成“鸡爪样”,周围肿瘤细胞呈放射状排列。
关键鉴别诊断指标
•与星形细胞瘤的区分:
•少突细胞核圆整、空晕明显,星形细胞核则呈梭形或不规则;
•GFAP(胶质纤维酸性蛋白)染色:少突细胞仅弱阳性,星形细胞强阳性。
•钙化的病理意义:钙化沿血管壁沉积呈“弯曲条带状”,是少突型的标志,但无分级提示价值。
分子病理:诊断与预后的核心
必检分子标志物
1.1p/19q共缺失:
•机制:1p缺失导致Notch通路失调,19q缺失影响Tumor Protein p53调控;
•临床价值:共缺失者对化疗敏感(PCV方案有效率>60%),中位生存期延长4.3年。
2.IDH突变:
•分型意义:IDH1 R132H突变阳性率>80%,无突变者需排除转移瘤。
新兴标志物
•TERT启动子突变:与1p/19q缺失共存时提示预后更好,单发则可能促进间变转化。
•MGMT甲基化:虽非少突型特异性标志,但甲基化者对替莫唑胺响应率提升2倍。
影像与病理的关联性
CT与钙化的诊断价值
•钙化模式:弯曲条带状或脑回样钙化是少突型的典型征象(发生率70%-90%),而星形细胞瘤钙化多呈斑点状。
•位置提示:额叶皮质下钙化灶伴颅骨内板侵蚀,强烈提示少突型而非脑膜瘤。
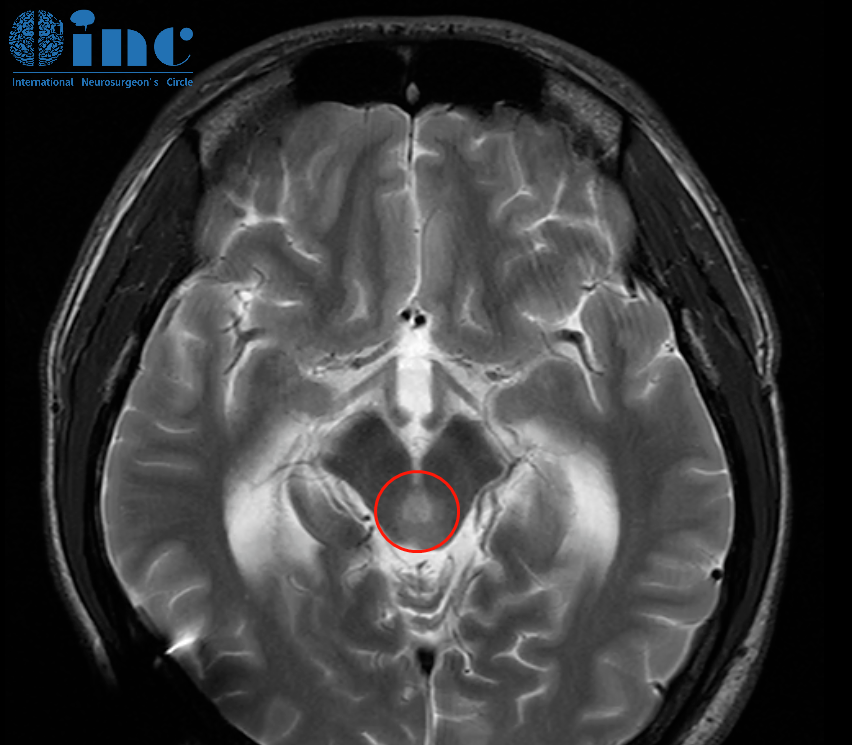
MRI的功能补充
•T2/FLAIR序列:高信号区反映肿瘤浸润范围,但无法区分Ⅱ级与Ⅲ级。
•增强扫描意义:Ⅲ级肿瘤可见斑片状强化(血脑屏障破坏),而Ⅱ级通常无强化。
病理诊断流程的标准化
术中冰冻切片(IFS)的局限
IFS对少突型诊断准确率仅54.6%-69.7%,因冷冻无法呈现蜂窝状结构,易误诊为星形细胞瘤。关键策略:术中优先送检钙化区域提高检出率。
分子检测的时机与方法
•必检场景:
•所有疑似少突胶质细胞瘤的活检标本;
•混合性胶质瘤需明确优势成分。
•技术选择:
•FISH(荧光原位杂交)检测1p/19q:敏感性95%,但无法区分缺失机制;
•二代测序(NGS)同步分析IDH/TERT/MGMT。
病理分型对治疗与预后的影响
治疗响应差异
•1p/19q共缺失型:
•化疗敏感性:PCV方案(丙卡巴肼+洛莫司汀+长春新碱)使5年生存率达74.5%(95%CI:70.1-78.9%);
•放疗可延迟:年轻患者术后无症状可暂缓放疗。
•IDH野生型:即使组织学符合Ⅱ级,生物学行为类似Ⅳ级,需早期放化疗。
生存预测模型
基于中国脑胶质瘤协作组数据(2023),预后公式为:
预后指数=0.5×(年龄>50岁)+0.8×(部分切除)+1.2×(无1p/19q缺失)
指数>1.5者5年生存率<40%,需强化治疗。
常见问题答疑
Q1:病理报告中的“蜂窝状结构”一定是少突胶质细胞瘤吗?
并非绝对!甲醛固定后的人为假象可模拟该结构,需结合1p/19q检测确认。星形细胞瘤偶见类似表现。
Q2:为什么钙化如此常见?
因肿瘤分泌碱性磷酸酶呀!该酶促进钙盐沿血管沉积,形成条带状钙化。但钙化程度与恶性度无关。
Q3:1p/19q缺失如何影响治疗选择?
缺失者对化疗敏感,首选PCV方案而非替莫唑胺。研究显示PCV使中位生存期延长至14.7年,远超替莫唑胺的10.2年。
Q4:术后病理升级(Ⅱ级→Ⅲ级)常见吗?
约35%的Ⅱ级病例术后5年内升级。若Ki-67>5%或TERT突变阳性,建议3个月复查一次MRI。
Q5:混合型少突星形细胞瘤的病理诊断难点?
难点在界定优势成分!需同时满足:①GFAP阳性细胞<30%;②1p/19q缺失。否则归为星形型。
Q6:儿童会得少突胶质细胞瘤吗?
罕见(<5%)!儿童患者需优先检测BRAF融合基因,因其更可能是毛细胞型星形细胞瘤。
Q7:分子检测未检出1p/19q缺失,但组织学符合怎么办?
需重新评估IDH状态!IDH突变型可能为星形细胞瘤;若IDH野生型则提示高级别转化,预后较差。推荐阅读:少突胶质细胞瘤百科
- 文章标题:少突胶质细胞瘤的病理是什么?关键特征和分析一文看懂
- 更新时间:2025-08-25 16:35:43

 400-029-0925
400-029-0925