自20世纪90年代初复兴以来,神经内镜技术已在全球多个中心迅速发展。神经内镜技术的目标是以最小的手术创伤提供有效的治疗。这可以通过精心规划手术入路、使用神经导航等技术辅助工具,以及使用合适的神经内镜设备来实现。
内镜鞘的实用性在文献中报道不足。对鞘管的批评之一是其锋利的边缘以及相应的神经血管损伤风险。作为替代方案,一些外科医生主张使用可剥离鞘。
INC国际内镜大咖、世界神经外科学会联合会(WFNS)内镜委员会前主席Henry W.S.Schroeder(施罗德)教授发表研究《Benefits of Endoscopic Sheath in Intraventricular Neuroendoscopy:Technical Note》,阐释了内镜鞘的使用方法并展示了其优势。自2007年以来,施罗德教授等在约300例脑室内神经内镜手术中使用了LOTTA脑室镜系统,并认为鞘管是脑室镜系统的重要组成部分。

这里我们特别提一下LOTTA脑室镜,LOTTA脑室镜的诞生,源自施罗德教授的卓越智慧。作为国际神经内镜领域的大咖,施罗德教授凭借数十年的临床经验与创新精神,发明了这款兼具高精度与微创性的脑室镜系统。有趣的是,“LOTTA”这个名称正是取自Schroeder教授爱女的名字,让这项技术更添温情。点击阅读:不开颅,怎么“钻”进大脑取瘤?LOTTA脑室镜发明者破解脑室手术难题!
内镜鞘的功能应用
1.系统构成与基本置入技术
LOTTA脑室镜系统由脑室镜主体、内镜鞘、套管针及光学套管针四部分构成。内镜鞘可在徒手操作或神经导航引导下,借助套管针经颅钻孔引入脑室系统或其他囊性腔隙。
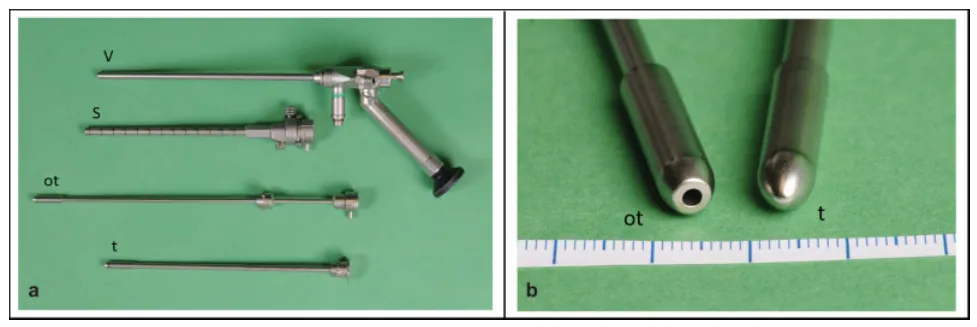
(a)LOTTA脑室镜系统及其组件,包括脑室镜、内镜鞘、套管针和光学套管针。(b)光学套管针带有可置入1.2毫米0度柱状镜内镜的通道。缩写:ot,光学套管针;S,内镜鞘;t,套管针;V,脑室镜。
对于室间孔狭小的患者,推荐使用内含1.2毫米0度内镜的光学套管针进行辅助引导。其优点在于能够在入路过程中实时显示腔内结构,即时识别进入目标腔隙的时机,同时可将小的室间孔扩张约1毫米,以便鞘管顺利通过。具体操作步骤为:在内镜直视下,将带有光学套管针的鞘管精准定位于小室间孔的中央,随后借助套管针尖端的锥形设计缓慢推进至第三脑室内,室间孔因此得以渐进性扩张而不损伤穹窿结构。
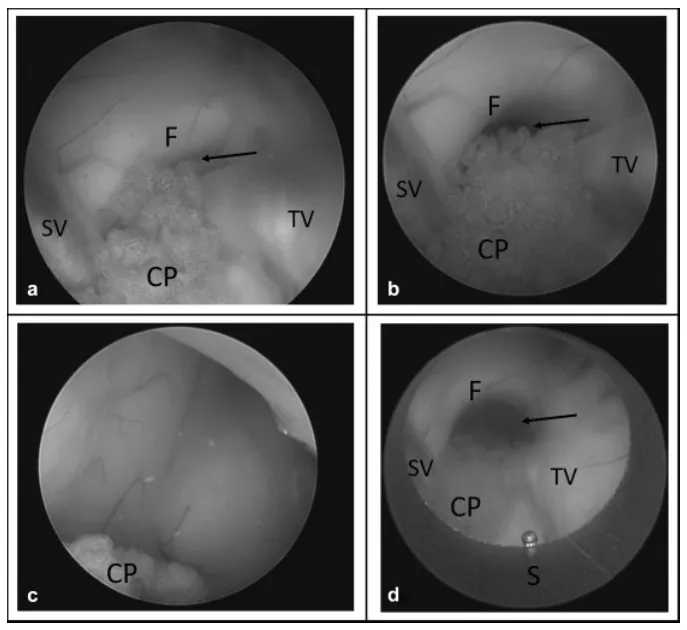
使用光学套管针及鞘管扩张小型室间孔。(a)室间孔过小,无法通过鞘管。在内镜直视下,将鞘管定位于室间孔中央,随后小心向前推进至第三脑室内。将鞘管退回到侧脑室后,可见扩张后的室间孔及结构完整的穹窿。箭头指示室间孔。缩写:CP,脉络丛;F,穹窿;S,内镜鞘;SV,隔静脉;TV,丘纹静脉。
若室间孔无需扩张,但其相对于鞘管外径仍显狭小时,可将内镜向鞘管内回缩3至4毫米,使鞘管边缘在镜头前方清晰显露,在直视监控下引入内镜鞘,从而有效避免对穹窿、脉络丛及周围静脉的意外损伤。
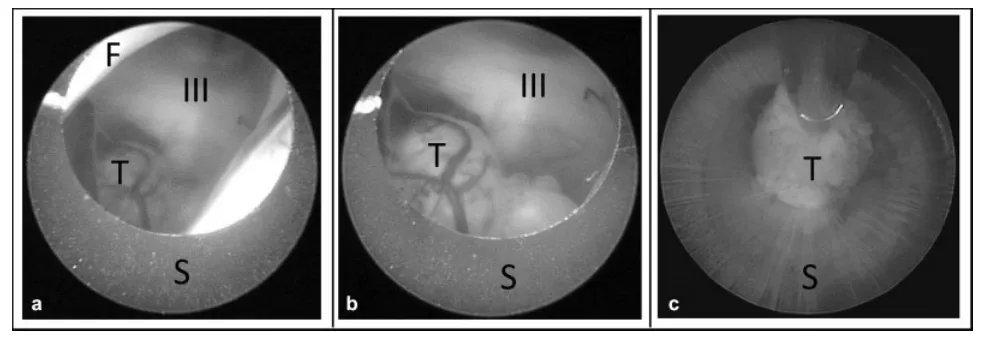
(a)为观察鞘管边缘,将内镜向鞘管内回缩。(b)随后,在内镜直视下(观察穹窿、静脉及脉络丛以避免意外损伤),将鞘管引入第三脑室。(c)若肿瘤碎块过大无法通过主工作通道,术者可钳住肿瘤碎块,将其连同整个脑室镜一起从留置在脑内的鞘管中取出。缩写:III,第三脑室;F,穹窿;S,内镜鞘;T,肿瘤。
2.保护脑组织与神经血管结构
内镜鞘最基本的功能是在内镜进出脑室过程中保护穿刺通道周围的脑实质。在无鞘操作模式下,若需反复取出并重新置入内镜——例如在肿瘤碎块切除过程中——每次重新穿刺均会对穿刺通道周围的脑组织造成刺激和潜在损伤,且此类损伤往往在术后才能通过影像学发现。内镜鞘的留置使内镜可反复进出脑室而无需重建穿刺通道,从根本上消除了这一风险。
此外,当内镜鞘留置于小室间孔内时,鞘管外壁对穹窿形成环周保护,同时容许各类内镜及操作器械自由进出,这对于室间孔狭小而手术操作频繁的病例具有重要意义。在内镜下第三脑室底造瘘术中,LITTLE LOTTA脑室镜的小口径鞘管还可用于保护基底动脉及其穿支,减少器械操作时对深部血管的直接接触风险。
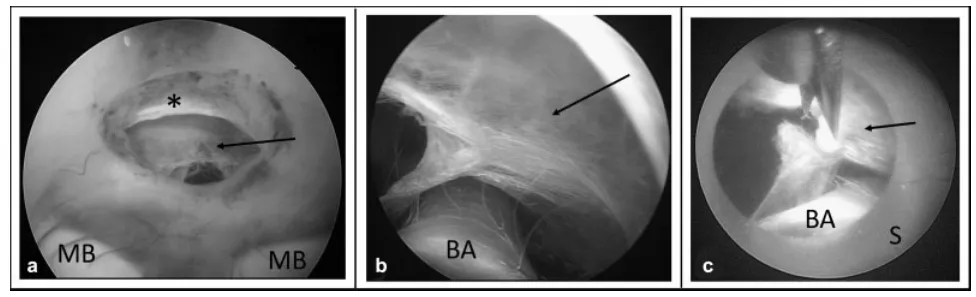
合并桥前蛛网膜的内镜下第三脑室造瘘术。(a)第三脑室造瘘术后,透过宽敞的脑室造瘘口及已开窗的Liliequist膜可见深部蛛网膜。(b)将LITTLE LOTTA脑室镜的鞘管经脑室造瘘口向前推进后,可见基底动脉及蛛网膜。(c)在内镜鞘保护基底动脉的同时,用剪刀切开蛛网膜。箭头指示桥前蛛网膜;星号指示Liliequist膜。缩写:BA,基底动脉;MB,乳头体;S,内镜鞘。
3.在狭窄脑室腔内创造有效工作空间
脑室系统因各种原因处于狭窄状态时,神经内镜操作面临工作空间严重不足的困境,器械自由度受限,手术难度倍增。内镜鞘的独特优势在于,当鞘管置入脑室后,将脑室镜向鞘管内适度回缩,即可在鞘管远端前方创造出额外的工作空间,使外科医生能够以更大的操作角度和器械运动范围完成复杂的脑室内解剖与病灶处理。
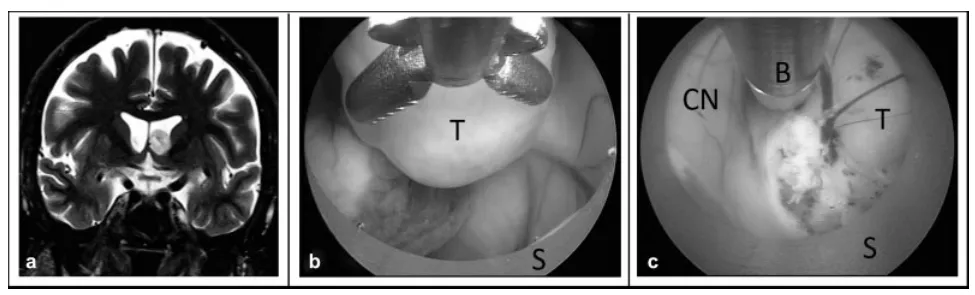
狭窄脑室内的内镜肿瘤切除术。(a)冠状位T2加权磁共振图像显示侧脑室内肿瘤,脑室空间狭小。(b)将内镜向鞘管内回缩,以创造额外工作空间。(c)使用鞘管将肿瘤从尾状核牵开,以便显露肿瘤基底并用双极电凝处理。缩写:B,双极电凝电极;CN,尾状核;S,内镜鞘;T,肿瘤。
4.牵开神经血管结构
内镜鞘亦可作为轻柔的组织牵开工具,在脑室内手术中发挥关键作用。在多例胶样囊肿切除术中,鞘管被用于温和牵开穹窿,以充分显露起源于脉络膜组织的囊蒂血管。在脑室内肿瘤切除术中,鞘管可协助将肿瘤从脑室壁上牵离,为双极电凝处理肿瘤附着于尾状核处的供血血管提供清晰的操作视野。
与常规组织牵开器相比,内镜鞘进行牵开操作具有以下特点:牵开力量柔和可控;鞘管内镜同步配合,可在牵开状态下保持清晰成像;且牵开本身不占用额外的操作通道,有效减少了器械干扰。
5.术中出血的处理
术中出血是神经内镜手术中最棘手的并发症之一。传统的处理手段包括持续冲洗、双极电凝及人为创造干燥视野等。内镜鞘为上述技术提供了更为有效的实施平台:将脑室镜在鞘管内适度回缩,可在镜头前方形成一个相对封闭的小空间,通过持续灌注冲洗液,该区域能够维持无血状态;随后可将鞘管缓慢地引导至出血点附近,在清晰视野下精准识别出血血管,再经主工作通道置入双极电凝探头对出血点实施电凝止血。这一操作路径将鞘管的导引功能、冲洗空间的维持功能与电凝器械的精准定位有机结合,显著提升了术中止血的可控性与安全性。
6.扩大有效工作通道
通道内镜的固有局限之一在于主工作通道口径较小,当切除体积较大的肿瘤或囊肿时,碎块可能无法顺利经主通道取出。内镜鞘为解决这一问题提供了简洁有效的方案:外科医生可用抓钳夹持较大的肿瘤碎块,将内镜与碎块一并从留置于脑内的鞘管中整体撤出,此时主工作通道被等效扩展至鞘管的完整内径,从而实现较大碎块的顺利取出。同样,漂浮于脑脊液中难以钳夹的细小碎片,可利用鞘管进行汇聚捕获,再整体取出,操作便捷,显著减少了器械进出脑室的次数。
典型案例:第三脑室胶样囊肿切除术
一名55岁男性患者因进行性行走障碍与记忆力减退就诊,影像学检查提示脑积水。头部磁共振成像(MRI)进一步明确为第三脑室胶样囊肿伴梗阻性脑积水。由施罗德教授主刀,为该患者施行了神经内镜下第三脑室胶样囊肿切除术。术后三年随访显示囊肿完全切除,无复发。
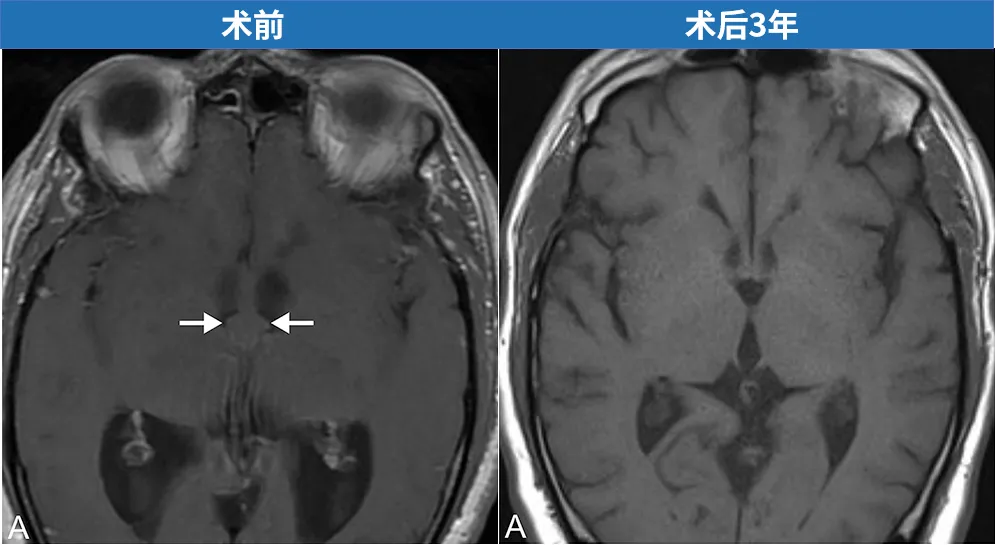
术前磁共振成像显示胶样囊肿,导致双侧脑室积水。
手术技术
手术最佳穿刺点借助神经导航系统确定。手术首先电凝脉络丛及囊壁血管,随后切开囊肿壁并吸除囊内容物。囊肿排空后,用抓钳夹持囊膜并将其轻柔地牵拉至侧脑室内。需特别注意对侧脉络丛与囊肿粘连的情况,在完全游离囊肿前,需先将该处脉络丛电凝并切断。
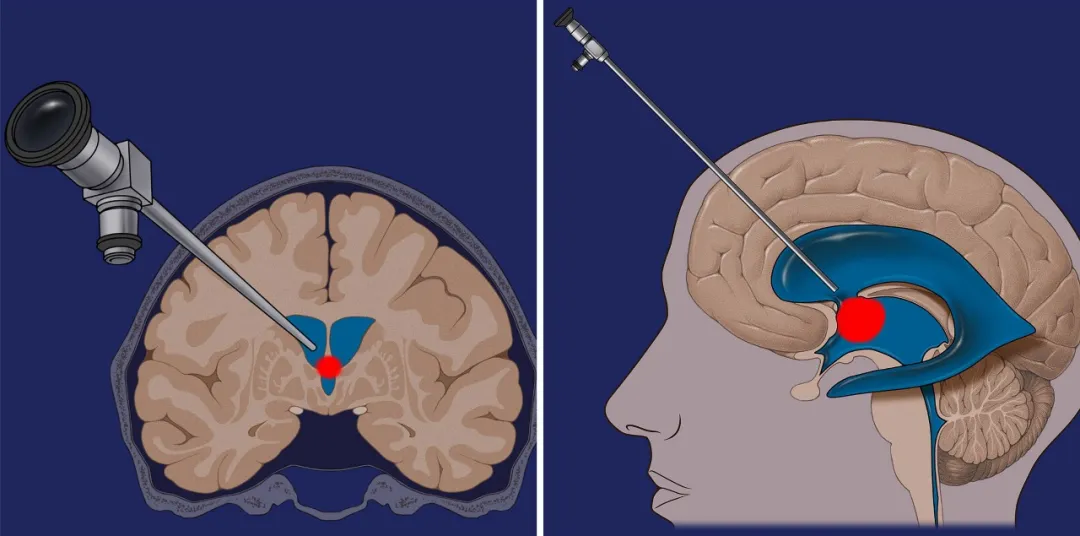
图:根据磁共振成像(MRI)规划手术入路,手术轨迹绕过尾状核头。
在该案例中,施罗德教授在导航引导下将带有鞘管的LOTTA脑室镜(Karl Storz SE&Co.KG)连同穿刺针一并引入侧脑室额角。
通过LOTTA脑室镜的一个侧方通道,用微型抓钳提起囊膜,以显露连接囊肿与第三脑室脉络膜组织的囊蒂。随后,经主工作通道置入双极电凝探头,对囊蒂内的血管进行电凝处理。之后用显微剪刀离断囊蒂,完整切除囊肿。
手术结束前,使用30度及45度诊断性内镜仔细检查脑室系统,确认无囊肿残留,并排除囊内实性成分堵塞中脑导水道的可能。钻孔处以明胶海绵填塞,帽状腱膜予以严密缝合,皮肤采用无创伤缝线连续缝合。
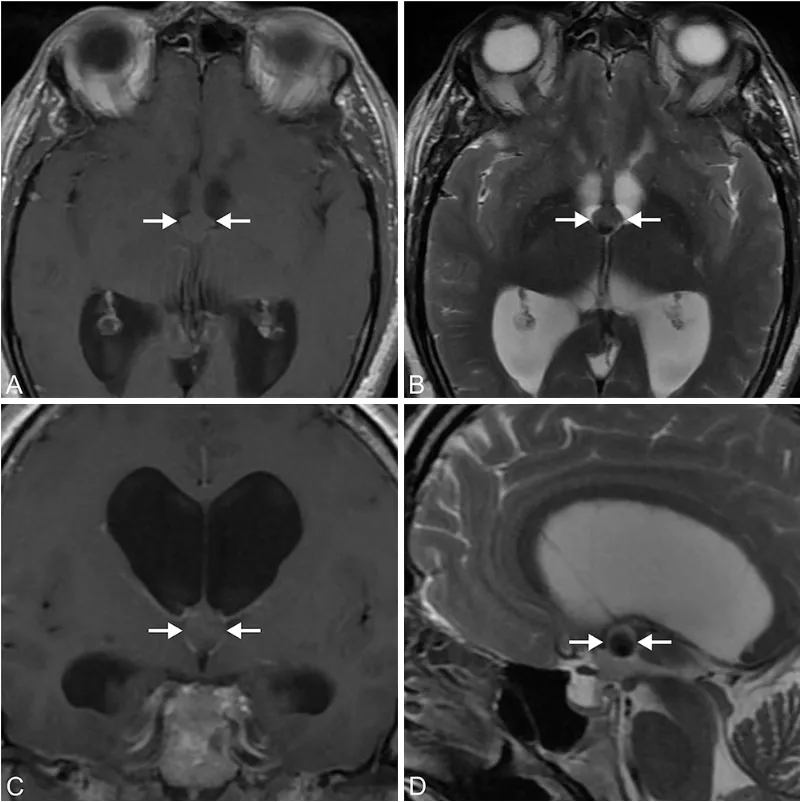
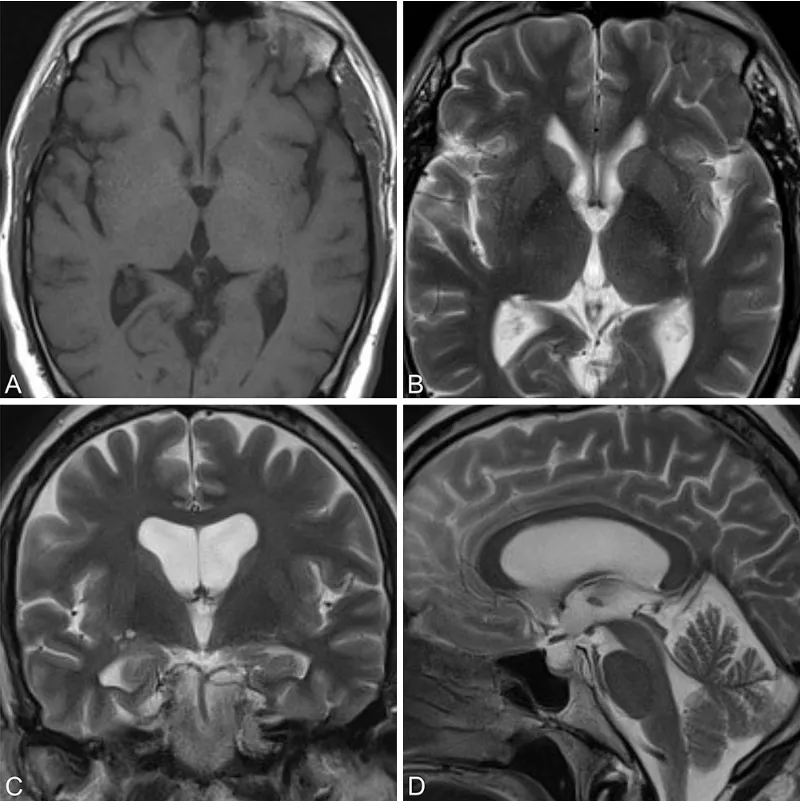
术后3年复查MRI(T1加权轴位A,T2加权轴位B、冠状位C、矢状位D)显示囊肿全切,无残留与复发征象,脑室系统形态恢复良好。
讨论
本报告强调了内镜鞘在脑室内神经内镜手术中的实用性,并描述了其使用方法。多次无鞘重新置入内镜会增加周围结构损伤的风险,这种损伤可能在术后才被发现。10虽然可剥离鞘也能保护脑组织,但像内镜鞘那样精确引导可剥离鞘几乎是不可能的。与可剥离鞘相比,内镜鞘可以作为一种动态工具使用。它可以在脑室系统内移动,内镜也可以在鞘管内移动。借助这两种移动的可能性,外科医生可以利用本报告中描述的内镜鞘的所有功能。内镜鞘的一个缺点是其锋利的边缘。因此,神经内镜医生需要注意不要将鞘管垂直推压在神经血管结构上。根据我们的经验,鞘管尖端的锋利边缘从未成为问题。
神经内镜中使用鞘管显然有助于保护周围的脑组织。可剥离鞘最初是为神经内镜以外的适应症开发的。内镜鞘是专门为脑室内神经内镜手术开发的。它不仅是插入内镜进入脑室的可剥离鞘的替代品,更是一种用于牵开和止血的手术工具。正确使用鞘管应能减少损伤并提高神经内镜的操作灵活性。因此,我们推荐在脑室镜手术中使用它。
- 文章标题:300例脑室内神经内镜手术证实:正确使用这套器械,术中出血、通道受限迎刃而解
- 更新时间:2026-03-26 10:48:28

 400-029-0925
400-029-0925