在神经外科学的临床实践与研究领域中,脑干胶质母细胞瘤(Brainstem Glioblastoma, BSG)作为极具挑战性的神经系统肿瘤,其诊疗难题始终备受学界关注。该肿瘤起源于脑干这一维系人体基本生命活动的核心解剖区域,因兼具特殊的神经解剖位置与高度侵袭性的生物学行为,成为严重威胁患者生命健康的重大疾病。临床数据显示,脑干胶质母细胞瘤不仅显著缩短患者生存期,且其高复发特性极大增加了临床治疗的复杂性与难度;与此同时,该疾病的遗传相关性研究亦处于不断探索与深化阶段。系统剖析影响脑干胶质母细胞瘤患者生存期的相关因素,有助于建立科学的疾病预后评估体系;深入探究肿瘤复发机制可为临床干预策略的优化提供理论依据;而阐明其遗传背景特征则为早期筛查预警及精准医疗方案的制定奠定基础。我们拟从生存期影响因素、复发机制及遗传关联三个维度,对脑干胶质母细胞瘤展开系统性综述,以期为临床诊疗及基础研究提供全面的理论参考。
相关阅读:脑干胶质母细胞瘤

一、脑干胶质母细胞瘤的生存期
脑干胶质母细胞瘤患者的生存期受多种因素交织影响,涉及肿瘤自身特性、治疗干预手段以及患者个体状况等多个层面,这些因素相互作用,共同决定着患者生命的长度。
(一)肿瘤自身特性
肿瘤的病理分级直接关乎患者的预后。在世界卫生组织(WHO)中枢神经系统肿瘤分类中,脑干胶质母细胞瘤多被归为 IV 级,这意味着肿瘤细胞具有高度异型性,增殖速度极快,且侵袭能力极强。此类肿瘤细胞会迅速侵犯周围正常脑组织,破坏脑干的神经传导功能,导致病情急剧恶化。与低级别胶质瘤相比,IV 级脑干胶质母细胞瘤患者的生存期显著缩短。
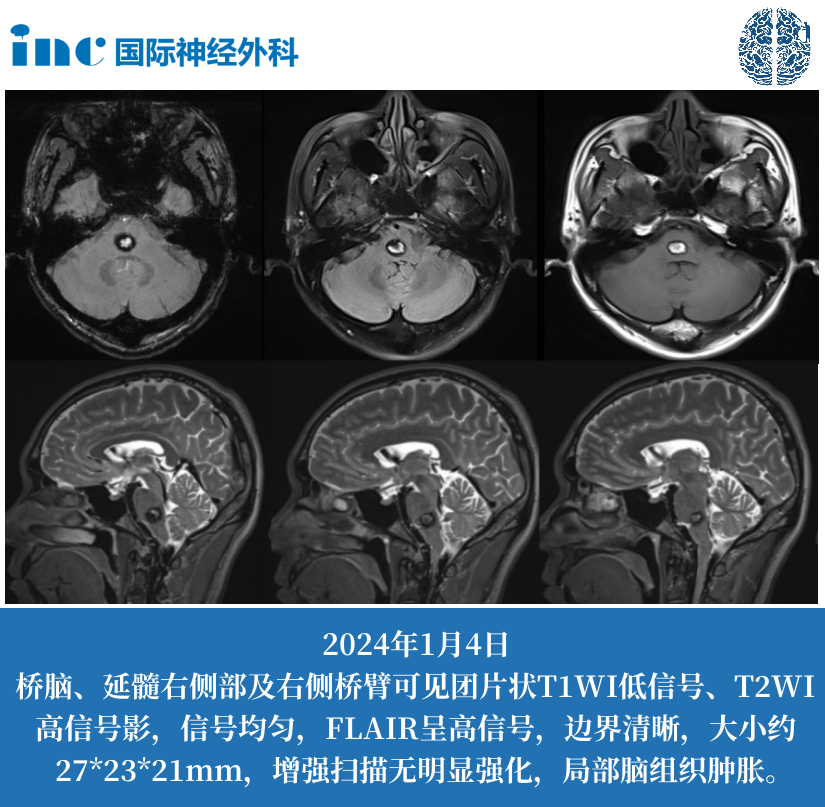
肿瘤的生长部位同样对生存期有着关键影响。脑干由中脑、脑桥和延髓组成,各个部位功能至关重要。中脑负责眼球运动、瞳孔调节等功能;脑桥参与呼吸、睡眠等生命活动调节;延髓更是心跳、呼吸等基本生命中枢所在。当肿瘤位于延髓等关键部位时,即使肿瘤体积较小,也可能直接压迫生命中枢,导致呼吸、心跳骤停等严重后果,极大缩短患者生存期;而生长在相对 “边缘” 区域的肿瘤,对生命体征的威胁相对较缓,患者生存期可能相对较长。
肿瘤的大小和扩散程度也是影响生存期的重要因素。体积较大的肿瘤,往往已经对周围神经结构造成广泛侵犯和破坏,手术难以完全切除,残留的肿瘤细胞会继续生长,加速病情进展;而肿瘤一旦发生扩散,转移至脑干其他部位或远处脑组织,治疗难度呈指数级上升,患者生存期也会随之大幅缩短。
(二)治疗干预手段
手术治疗是脑干胶质母细胞瘤治疗的重要环节,但由于脑干结构精细复杂,手术风险极高,稍有不慎就可能损伤重要神经核团和传导束,导致患者出现严重的神经功能障碍甚至死亡。因此,在多数情况下,手术难以实现肿瘤的完全切除,只能尽可能切除部分肿瘤组织,降低肿瘤负荷。即便如此,手术对于缓解肿瘤对周围脑组织的压迫、改善患者症状仍有一定作用,而手术切除程度与患者生存期密切相关,切除程度越高,患者生存期可能越长。
术后的放疗和化疗同样对患者生存期影响深远。放射治疗可以通过高能射线杀灭残留的肿瘤细胞,抑制肿瘤复发。目前常用的调强放射治疗(IMRT),能够精准地照射肿瘤区域,在保证治疗效果的同时,减少对周围正常脑组织的损伤。化疗药物如替莫唑胺,可通过血 - 脑屏障进入肿瘤组织,干扰肿瘤细胞的 DNA 合成,发挥抗肿瘤作用。联合放疗和化疗的综合治疗方案,相比单一治疗方法,能够显著延长患者的生存期。近年来新兴的肿瘤电场治疗(TTFields),通过产生交变电场干扰肿瘤细胞有丝分裂,与放化疗联合使用,也为提高患者生存期带来了新的希望。
(三)患者个体状况
患者的年龄和身体基础状况对生存期影响显著。年轻患者身体机能和耐受性较好,能够更好地承受手术、放疗和化疗带来的副作用,治疗效果相对更佳,生存期也相对较长;而老年患者身体机能衰退,常合并多种基础疾病,如高血压、糖尿病、心脏病等,这些基础疾病不仅增加了治疗风险,还会影响患者对治疗的耐受性和恢复能力,导致治疗效果不佳,生存期缩短。
患者的心理状态也与生存期息息相关。积极乐观的心态有助于提高患者的免疫力,增强对疾病的抵抗力,使其更好地配合治疗,从而对预后产生积极影响;长期焦虑、抑郁等不良情绪则会抑制机体免疫系统功能,影响患者生活质量和治疗效果,进而缩短生存期。因此,关注患者心理状态,给予心理支持和干预,对延长患者生存期至关重要。
综合多种因素,脑干胶质母细胞瘤患者的平均生存期通常较短,多数患者在确诊后生存期仅为 12 - 18 个月左右,但也有少数患者通过积极有效的治疗和良好的个体状况,生存期能够得到显著延长。
二、脑干胶质母细胞瘤的复发率
脑干胶质母细胞瘤的复发率居高不下,这一特性严重影响着患者的治疗效果和预后,其背后有着复杂的生物学机制和治疗相关因素。
(一)肿瘤生物学特性
脑干胶质母细胞瘤细胞具有极强的侵袭性和迁移能力,肿瘤细胞会像树根一样向周围正常脑组织浸润生长,与正常组织界限模糊。在手术过程中,很难将这些浸润到正常组织中的肿瘤细胞完全清除,残留的肿瘤细胞就成为日后复发的根源。而且,这些肿瘤细胞具有高度的异质性,不同部位的肿瘤细胞在基因表达、代谢特点等方面存在差异,部分肿瘤细胞可能对放疗、化疗产生耐药性,导致治疗后肿瘤细胞再次增殖复发。
肿瘤干细胞的存在也是复发的重要原因。肿瘤干细胞具有自我更新和多向分化的能力,对常规的放化疗不敏感,能够在治疗后存活下来。当机体环境适宜时,肿瘤干细胞会再次分化增殖,形成新的肿瘤病灶,导致肿瘤复发。研究表明,脑干胶质母细胞瘤中肿瘤干细胞的比例相对较高,这也是其复发率高的关键因素之一。
(二)治疗相关因素
如前文所述,由于脑干的特殊解剖结构,手术难以实现肿瘤的根治性切除。即使采用先进的手术技术,如术中磁共振成像(iMRI)、神经导航等辅助设备,也只能尽量切除可见的肿瘤组织,无法完全清除所有肿瘤细胞。残留的肿瘤细胞在术后会继续生长,导致肿瘤复发。
放疗和化疗虽然能够杀灭部分肿瘤细胞,但也存在局限性。放疗的剂量受到周围正常脑组织耐受程度的限制,无法给予肿瘤区域过高的剂量,这就可能导致部分肿瘤细胞无法被彻底杀灭;化疗药物在进入人体后,由于血 - 脑屏障的存在以及肿瘤细胞的耐药性等问题,难以在肿瘤组织中达到有效的治疗浓度,影响治疗效果,使得肿瘤细胞有机会再次增殖复发。
(三)监测和随访不足
脑干胶质母细胞瘤治疗后的监测和随访至关重要,但在实际临床中,部分患者由于各种原因未能严格按照医嘱进行定期复查。肿瘤复发早期往往没有明显症状,若不能及时通过影像学检查等手段发现复发迹象,错过最佳治疗时机,肿瘤会迅速进展,增加后续治疗难度,进一步提高复发率和降低患者生存率。
综合以上因素,脑干胶质母细胞瘤的复发率高达 70% - 80% 以上,且复发后的肿瘤恶性程度可能进一步增加,治疗难度更大,患者预后更差。

三、脑干胶质母细胞瘤的遗传性
脑干胶质母细胞瘤的遗传性一直是医学研究的重要方向,虽然大部分病例属于散发性,但遗传因素在部分患者发病过程中仍发挥着重要作用。
(一)明确的遗传性疾病相关
一些遗传性疾病与脑干胶质母细胞瘤的发生密切相关。例如,神经纤维瘤病 1 型(NF1)是一种常染色体显性遗传性疾病,患者体内 NF1 基因突变,导致神经嵴细胞发育异常,患神经系统肿瘤的风险显著增加,其中就包括脑干胶质母细胞瘤。此外,神经纤维瘤病 2 型(NF2)患者由于 NF2 基因突变,也容易发生中枢神经系统肿瘤,脑干胶质母细胞瘤在这类患者中也时有发生。李 - 法梅尼综合征患者因 TP53 基因突变,同样具有较高的患脑干胶质母细胞瘤的风险。这些遗传性疾病导致患者从出生起就携带了肿瘤易感基因,在后天环境因素的作用下,更容易发生肿瘤。
(二)遗传位点与易感基因研究
除了与明确遗传性疾病相关的基因突变,近年来的全基因组关联研究(GWAS)发现了多个与胶质母细胞瘤发病风险相关的遗传位点。这些位点可能通过影响基因的表达调控、细胞信号传导通路等机制,参与肿瘤的发生过程。虽然单个遗传位点对发病风险的影响相对较小,但多个遗传位点的累积效应,可能显著增加个体患脑干胶质母细胞瘤的可能性。例如,某些基因位点的变异可能影响 DNA 修复能力,使得细胞更容易积累基因突变,从而增加肿瘤发生风险;还有些基因位点可能与肿瘤细胞的增殖、侵袭能力相关。
不过,需要明确的是,即使携带这些遗传位点或易感基因,也并不意味着一定会患上脑干胶质母细胞瘤,遗传因素只是增加了患病的风险,疾病的发生还需要环境因素等多种因素的共同作用。
(三)遗传检测的意义
对于有脑干胶质母细胞瘤家族史的人群,进行遗传检测具有重要意义。通过检测相关的遗传性疾病基因和易感基因,可以早期发现潜在的肿瘤易感个体,采取更积极的预防措施,如定期进行神经系统检查和头部影像学检查,以便早期发现病变,做到早发现、早诊断、早治疗。同时,遗传检测结果也有助于医生为患者制定更个性化的治疗方案,例如对于携带特定基因突变的患者,可以选择更有针对性的靶向治疗药物,提高治疗效果。
四、脑干胶质母细胞瘤相关问题延伸问答
(一)脑干胶质母细胞瘤患者如何提高生存期?
提高脑干胶质母细胞瘤患者生存期需要多方面努力。首先,积极配合规范的综合治疗至关重要,包括尽可能安全切除肿瘤的手术,术后按医嘱进行放疗、化疗或肿瘤电场治疗等辅助治疗。其次,保持良好的生活方式,均衡饮食,摄入富含蛋白质、维生素和膳食纤维的食物,避免高脂肪、高糖、高盐饮食;适度进行身体锻炼,如散步、太极拳等,以增强身体机能和免疫力;规律作息,保证充足睡眠,有助于身体恢复。再者,重视心理调节,患者可通过与家人朋友交流、参加病友互助小组等方式,缓解心理压力,保持积极乐观的心态。此外,严格按照医生要求定期复查,及时发现病情变化并调整治疗方案,也对延长生存期至关重要。
(二)降低脑干胶质母细胞瘤复发率有哪些方法?
降低复发率首先要在手术中尽可能提高肿瘤切除程度,借助先进的手术技术和设备,减少肿瘤残留。术后规范进行放疗和化疗,通过放疗杀灭残留肿瘤细胞,化疗抑制肿瘤细胞增殖,同时可尝试联合新兴的肿瘤电场治疗等方法。此外,密切监测患者病情,定期进行头部影像学检查,如磁共振成像(MRI),及时发现微小的复发迹象并采取治疗措施。对于有条件的患者,还可进行肿瘤基因检测,根据基因特点选择合适的靶向治疗药物,精准抑制肿瘤细胞生长,降低复发风险。
(三)如何判断自己是否有脑干胶质母细胞瘤的遗传风险?
如果家族中有多人患有脑干胶质母细胞瘤或其他神经系统肿瘤,特别是存在神经纤维瘤病 1 型、神经纤维瘤病 2 型、李 - 法梅尼综合征等遗传性疾病患者时,自身遗传风险相对较高。这种情况下,可咨询专业医生,进行相关的遗传基因检测,通过检测特定的基因突变和遗传位点,评估患脑干胶质母细胞瘤的遗传风险。即使家族中没有明确的肿瘤病史,若自身出现不明原因的头痛、头晕、呕吐、视力下降、肢体无力、行走不稳等神经系统症状,也应及时就医检查,排除肿瘤可能。
(四)脑干胶质母细胞瘤的最新治疗研究有哪些进展?
在治疗研究方面,免疫治疗是当前热点。免疫检查点抑制剂如帕博利珠单抗、纳武利尤单抗等,通过解除肿瘤细胞对免疫系统的抑制,激活机体免疫细胞对肿瘤细胞的杀伤能力,部分临床试验已取得一定效果。肿瘤疫苗研发也在不断推进,通过激发机体特异性免疫反应,识别和攻击肿瘤细胞。此外,基于肿瘤基因特点的精准靶向治疗药物研发也有新突破,针对特定基因突变的靶向药物能够更精准地作用于肿瘤细胞,提高治疗效果,降低副作用。人工智能技术在脑干胶质母细胞瘤的诊断、治疗方案制定和预后预测等方面的应用也逐渐深入,有望为患者提供更精准、个性化的医疗服务。
- 文章标题:脑干胶质母细胞瘤生存期、复发率和遗传性?
- 更新时间:2025-06-15 05:45:44

 400-029-0925
400-029-0925