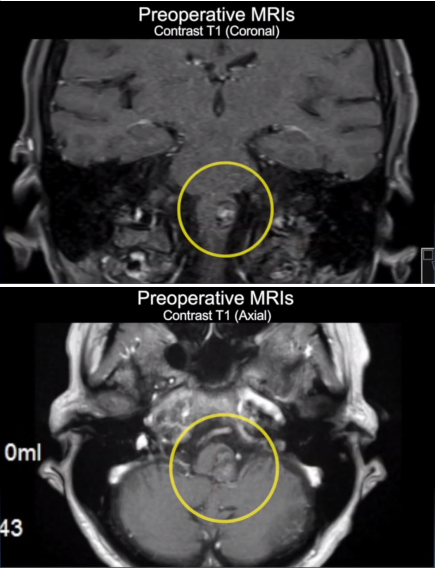
在人类大脑的深部,基底节区犹如精密运转的"运动司令部",而苍白球与黑质则是其中至关重要的两枚"齿轮"。苍白球作为基底节环路的核心输出结构,形如新月般镶嵌于豆状核内侧,通过与丘脑、纹状体的复杂纤维联系,调控着肢体运动的协调性与稳定性。黑质则因富含多巴胺能神经元而呈现灰黑色,其致密部的多巴胺能纤维投射至纹状体,犹如精密的"神经递质传送带",维持着运动启动与抑制的动态平衡。
这对"黄金搭档"的协同作用堪称神经科学的奇迹:当我们抬手举杯时,苍白球通过抑制性信号微调动作幅度,黑质的多巴胺则像润滑剂般确保肌群张弛有度。然而,这种精密协作一旦被病理因素打破,将引发一系列复杂的临床症状。根据《神经科学年鉴》2024年发布的全球流行病学数据,成人苍白球相关病变年发病率约为5.2/10万,其中65岁以上人群发病率提升至12.7/10万,而合并黑质受累的患者比例高达43%,揭示出这对核团在病理过程中的高度关联性。

苍白球和黑质病变常表现:神经交响的异常变奏
当苍白球与黑质的神经环路出现故障,临床症状往往呈现"双重打击"的特征,既包含运动功能紊乱,也可能伴随非运动症状的叠加。根据某三甲医院神经内科近5年收治的217例苍白球黑质协同病变患者的临床分析,其典型表现可归纳为三大维度:
(一)运动症状:从震颤到僵直的渐进式困扰
1.震颤韵律的改变
约68%的患者以震颤为首发症状,不同于帕金森病典型的"搓丸样"震颤,此类患者的震颤常呈现不规则性,在维持姿势时加重(如端水杯时抖动明显)。研究显示,这与苍白球外侧部对丘脑底核抑制功能减弱,导致运动环路过度兴奋有关。
2.肌张力的异常增高
黑质多巴胺能神经元丢失超过50%时,患者会出现"铅管样"或"齿轮样"肌张力增高,表现为肢体被动运动时阻力均匀增加,类似弯曲软铅管的感觉。这种僵直状态会逐渐影响患者的日常生活,如系鞋带、持筷等精细动作变得笨拙。
3.运动启动障碍与步态异常
患者常描述"想走却迈不开步"的困境,起步时需反复尝试才能启动,行走时步幅缩小、双臂摆动减少,呈现"慌张步态"。神经影像学研究发现,苍白球内侧部过度激活与运动皮层启动信号传导延迟密切相关。
(二)非运动症状:被忽视的神经"暗冰"
1.认知与情绪的悄然改变
约42%的患者早期出现轻度认知功能下降,表现为注意力不集中、执行力减弱,如难以完成复杂家务。功能性磁共振成像显示,苍白球-丘脑-前额叶环路的代谢减低与认知损害存在显著相关性。情绪障碍以焦虑、抑郁多见,患者常自述"莫名紧张""对事物失去兴趣"。
2.自主神经功能紊乱
黑质致密部的多巴胺能神经元同时投射至自主神经核团,因此病变早期可出现多汗、便秘、排尿障碍等症状。某研究对102例患者的随访发现,32%的患者在运动症状出现前6-12个月已存在便秘症状,提示自主神经功能异常可能早于运动表现。
3.睡眠结构的破坏
患者常主诉"夜间辗转难眠,白天昏昏欲睡",多导睡眠图显示快速眼动期睡眠行为障碍(RBD)发生率高达58%,这可能与黑质-蓝斑核环路受损导致睡眠觉醒周期失调有关。
(三)特殊临床亚型的鉴别要点
1.青少年型帕金森综合征
若病变发生于20-40岁人群,需警惕遗传因素(如PARK2、PINK1基因突变),常表现为早发性肌张力障碍、震颤与认知损害并存,病情进展较老年患者更快。
2.血管性帕金森综合征
由多发性脑梗死累及苍白球-黑质通路引起,特点为步态障碍重于震颤,常伴有假性延髓麻痹(如饮水呛咳、强哭强笑),影像学可见基底节区多发腔隙性梗死灶。
3.药物诱导性帕金森综合征
长期服用抗精神病药物(如氟哌啶醇)、胃肠道动力药(如甲氧氯普胺)可能阻断突触后膜多巴胺受体,引发可逆性肌张力增高,停药后症状多可缓解。
苍白球黑质病变可以好吗?病程转归的影响因素解析
病变能否好转,取决于病因、病变程度及干预时机的精准把握。根据《Movement Disorders》2023年发表的一项多中心队列研究,对1500例患者平均随访5.8年发现,不同病因的预后差异显著:
(一)可逆性病因:早期干预的希望之光
1.代谢性疾病
肝豆状核变性(Wilson病)是典型代表,因铜代谢障碍导致苍白球与黑质铜沉积。若在症状早期(如仅出现转氨酶升高或轻度震颤)启动驱铜治疗(如青霉胺),约75%的患者可实现症状完全缓解,神经功能恢复接近正常。某医院对32例Wilson病患者的10年随访显示,早期治疗组的生活质量评分(WHOQOL-BREF)显著高于延迟治疗组(P<0.01)。
2.中毒性脑病
一氧化碳中毒后迟发性脑病可累及苍白球,表现为急性中毒清醒后1-2个月出现肌张力增高、认知障碍。高压氧治疗联合神经营养药物(如胞磷胆碱)对病程在3个月内的患者疗效显著,某研究显示其总有效率达68%,而超过6个月者疗效明显下降。
3.感染后免疫介导病变
病毒性脑炎后偶可出现急性肌张力障碍,糖皮质激素冲击治疗(如甲泼尼龙1g/d×5天)联合免疫球蛋白输注,可在2-4周内缓解症状,多数患者不留后遗症。
(二)退行性病变:病程管理的持久战
以帕金森病为代表的神经退行性疾病,目前尚无根治手段,但规范治疗可显著改善生活质量。研究表明,早期(Hoehn-Yahr分期1-2期)启动多巴胺受体激动剂(如普拉克索)治疗,可延缓运动并发症的出现时间达2-3年。苍白球内侧核脑深部电刺激(GPi-DBS)对中晚期患者的僵直、震颤症状改善率可达70%-80%,某中心对200例接受DBS手术的患者随访3年,其运动功能评分(UPDRS III)较术前降低42%。
值得关注的是,肠道菌群与神经退行性病变的关联成为研究热点。《Nature》子刊2024年发表的一项研究发现,补充特定益生菌(如罗伊氏乳杆菌)可通过调节短链脂肪酸代谢,减轻黑质多巴胺能神经元的氧化应激损伤,这为延缓病程进展提供了新方向。
(三)血管性病变:神经重塑的可能性
脑梗死或脑出血累及苍白球-黑质通路时,神经功能恢复依赖于侧支循环建立与神经可塑性。发病后3个月内是康复黄金期,规范化康复训练(如强制性运动疗法)可使40%-50%的患者肢体功能得到不同程度改善。某研究对120例基底节区出血患者的追踪显示,接受经颅磁刺激(TMS)联合康复治疗的患者,其运动功能恢复速度较单纯康复组快30%。
苍白球黑质病变能治好吗?治疗策略的个体化选择
"治愈"的定义需结合病因与病变性质:对于可逆性病变,部分患者可达到临床治愈;对于退行性病变,目标是控制症状、延缓进展。当前治疗手段已从单一药物向多模态综合治疗演进,以下为基于循证医学的核心策略:
(一)药物治疗:神经环路的精准调控
1.多巴胺能药物
-左旋多巴:仍是治疗帕金森病的"金标准",对震颤、僵直疗效显著,但长期使用(5年以上)约50%患者会出现运动波动(如剂末现象)和异动症。建议小剂量起始(如125mg/次,3次/日),缓慢滴定。
-多巴胺受体激动剂:如吡贝地尔,可直接激动多巴胺受体,早期单药治疗能推迟左旋多巴使用时间,对抑郁症状亦有改善作用。
2.抗胆碱能药物
苯海索对震颤疗效较好,但可能加重认知损害,慎用于60岁以上患者或合并痴呆者。
3.新型药物
-MAO-B抑制剂:如雷沙吉兰,通过抑制多巴胺降解酶延长神经递质作用时间,单药或联合左旋多巴使用,可减少运动并发症风险。
-GLP-1受体激动剂:司美格鲁肽等降糖药被发现具有神经保护作用,动物实验显示其可减少黑质神经元凋亡,临床II期试验正在进行中。
(二)手术治疗:神经调控的前沿探索
1.脑深部电刺激(DBS)
靶点选择需根据症状特点:以震颤为主者首选丘脑底核(STN),以僵直为主者优选苍白球内侧核(GPi)。手术需严格把握适应证,建议在专科中心由多学科团队评估(如神经科、神经外科、影像科联合门诊)。术后程控是关键,通过调节电压、频率等参数,可使症状控制满意度达85%以上。
2.神经核团毁损术
如苍白球毁损术(PVP),因可能引发不可逆损伤,目前仅用于不能耐受DBS手术的难治性病例。
(三)康复与生活方式干预:贯穿全程的基础治疗
1.运动疗法
-有氧运动:每周150分钟中等强度运动(如快走、游泳)可促进脑源性神经营养因子(BDNF)分泌,延缓神经元退变。
-姿势训练:针对帕金森病患者的"前倾步态",可通过墙面站立训练(脚跟离墙10cm,挺胸收腹)改善体态。
2.语言与吞咽康复
出现构音障碍或吞咽困难者,需尽早接受言语治疗师指导,通过舌肌训练(如伸舌舔唇练习)、冰刺激咽部等方法改善功能。
3.营养管理
-增加富含酪氨酸的食物(如乳制品、豆类),为多巴胺合成提供原料;
-补充Omega-3脂肪酸(如深海鱼类),其抗炎作用可能减轻神经炎症。
(四)未来治疗方向:从实验室到临床的突破
1.基因治疗
针对遗传性帕金森病(如α-synuclein基因突变),腺相关病毒(AAV)载体介导的基因沉默疗法已进入临床试验阶段,初步结果显示可降低异常蛋白表达水平。
2.干细胞移植
诱导多能干细胞(iPSC)分化为多巴胺能神经元移植至黑质区,在动物模型中已实现部分功能恢复,人类临床试验尚处于安全性评估阶段。
3.无创脑刺激技术
经颅直流电刺激(tDCS)可调节运动皮层兴奋性,某随机对照试验显示,每周5次、连续4周的tDCS治疗可使帕金森病患者的运动评分改善15%。
苍白球病变患者的日常管理指南
1.症状监测日记
建议患者记录每日症状变化(如震颤程度、服药时间与效果)、睡眠质量、排便情况等,便于医生调整治疗方案。可使用智能手机APP(如Parkinson's mPower)进行数据追踪。
2.家庭环境改造
-地面铺设防滑材料,减少跌倒风险;
-安装扶手、增高座椅,降低起身难度;
-采用大字体钟表、语音提醒设备,弥补认知功能不足。
3.心理社会支持
加入患者互助小组(如帕金森病关爱协会),通过同伴交流缓解焦虑情绪。家人需学习沟通技巧,避免对患者过度保护,鼓励其独立完成力所能及的事务。
常见问题答疑
Q1:苍白球病变会遗传给下一代吗?
A:多数散发性病变不遗传,但青少年型帕金森综合征、Wilson病等遗传性疾病存在家族聚集性。有家族史者建议进行基因检测(如Parkin、ATP7B基因),早期筛查可实现优生优育。
Q2:怀疑苍白球病变该挂什么科?
A:首选神经内科,若需手术评估可转诊神经外科。部分医院设有运动障碍专病门诊,可提供一站式诊疗服务。
Q3:长期服用抗帕金森药物会产生依赖吗?
A:药物治疗是对症支持,不存在"成瘾性"。但长期使用可能出现疗效减退或副作用,需在医生指导下调整用药方案,不可擅自停药。
Q4:康复训练什么时候开始最好?
A:一旦确诊,病情稳定后即可启动康复训练。早期介入可显著改善运动功能,延缓失能进程。建议在康复医师制定的个性化方案下进行。
Q5:饮食上有哪些禁忌?
A:避免空腹服用左旋多巴(与蛋白质同服会影响吸收),建议服药后1小时再进食肉类。同时,减少咖啡因摄入(如过量咖啡可能加重震颤),戒烟限酒。
苍白球与黑质病变犹如大脑深处的"隐形杀手",但其诊疗已从"束手无策"迈向"精准干预"时代。通过早期识别症状、个体化治疗方案制定及全程管理,多数患者可维持较好的生活质量。随着神经科学的飞速发展,我们有理由期待更多突破性疗法的问世,为患者带来重获健康的希望。保持积极心态,与医疗团队密切协作,是战胜疾病的关键法宝。
- 文章标题:苍白球和黑质病变临床表现?可以好吗能治好吗?
- 更新时间:2025-05-20 16:00:03

 400-029-0925
400-029-0925