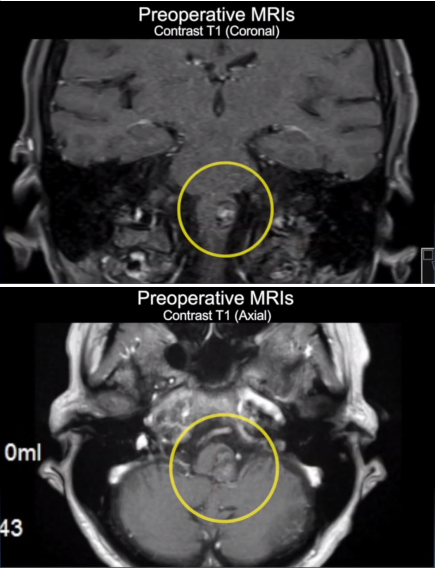
大脑作为人体的"指挥中枢",每一个细微结构的病变都可能引发复杂的功能异常。在大脑深部的基底神经节区域,有一对看似不起眼的灰质团块——苍白球,它如同精密仪器中的关键齿轮,在运动调控、情绪管理及认知功能中扮演着核心角色。当这一结构因各种病因出现病理改变时,所引发的临床症状往往具有多样性和复杂性,给诊断与治疗带来挑战。
大脑苍白球病变是什么病?
苍白球的解剖定位与生理功能
苍白球作为基底神经节的重要组成部分,位于大脑半球深部,具体位置在豆状核的内侧部,其外侧与壳核相邻,内侧紧邻内囊后肢。从解剖结构上,苍白球可分为外侧段(GPe)和内侧段(GPi),这种分区并非单纯的形态学划分,而是具有明确的功能差异:外侧段主要参与基底神经节的间接通路,与丘脑底核形成环路连接;内侧段则是基底神经节直接通路的关键输出结构,其纤维投射至丘脑腹前核与腹外侧核,进而调控大脑皮层的运动指令发放。
在神经生理功能方面,苍白球犹如一个精密的"运动滤波器",通过调节多巴胺能、GABA能及胆碱能等多种神经递质的平衡,对人体的随意运动进行精细调控。当苍白球功能正常时,它能有效抑制不必要的运动冲动,确保动作的协调性与流畅性。此外,现代神经影像学研究还发现,苍白球与边缘系统存在广泛的神经联系,参与情绪调节、奖赏机制及认知过程,这也解释了为何部分苍白球病变患者会出现情感障碍及执行功能下降等非运动症状。

常见致病因素与病理类型
苍白球病变的病因呈现显著的多样性,临床中可分为遗传性与获得性两大类,不同病因所致的病理改变及临床转归存在明显差异。
遗传性病因中,最具代表性的是神经退行性疾病,如亨廷顿病、肝豆状核变性(Wilson病)及神经铁沉积性疾病(如泛酸激酶相关神经变性病PKAN)。以肝豆状核变性为例,这是一种由ATP7B基因突变导致的铜代谢障碍性疾病,过量沉积的铜离子会选择性损害苍白球等基底神经节结构,病理切片可见神经元变性、胶质细胞增生及血管周围铜沉积。在神经铁沉积性疾病中,苍白球区域常出现异常的铁沉积,形成特征性的"虎眼征",这种铁过载会引发氧化应激反应,导致神经元凋亡。
获得性病因则涵盖了脑血管疾病、中毒、感染及医源性因素等。缺血性或出血性脑卒中若累及苍白球血供(其主要由豆纹动脉分支供血),可导致急性神经元坏死,形成软化灶;一氧化碳中毒时,苍白球对缺氧尤为敏感,易出现对称性坏死,这与该区域高代谢率及血脑屏障特点相关;某些药物如抗精神病药(典型抗精神病药)长期使用可能引发药源性苍白球损害,机制与多巴胺受体过度阻断有关;此外,罕见的中枢神经系统感染(如病毒性脑炎)也可能波及苍白球。
病理生理过程的现代认知
随着神经分子生物学的发展,对苍白球病变病理机制的认识已从单纯的形态学改变深入到分子信号通路层面。研究表明,无论是遗传性还是获得性因素,最终多通过氧化应激、线粒体功能障碍、兴奋性氨基酸毒性及炎症反应等共同通路导致苍白球神经元损伤。
在遗传性疾病中,基因突变可导致特定蛋白的结构或功能异常,如亨廷顿病中突变的huntingtin蛋白会在神经元内形成包涵体,干扰细胞器功能及基因表达;肝豆状核变性时铜离子的异常沉积会破坏线粒体呼吸链,产生大量氧自由基。而在获得性损伤中,缺血缺氧会引发ATP耗竭,导致细胞膜离子泵功能失调,细胞内钙超载激活一系列降解酶,同时血脑屏障破坏引发的炎症细胞浸润也会加重局部损伤。
值得关注的是,苍白球病变并非孤立事件,基底神经节环路的网络效应会使局部损伤产生广泛影响。例如,苍白球内侧段过度活跃会抑制丘脑-皮层通路,导致运动迟缓(如帕金森病样表现);而外侧段功能异常则可能解除对丘脑底核的抑制,引发异常运动模式(如肌张力障碍)。这种环路机制的紊乱是临床症状多样性的本质原因。
大脑苍白球病变症状表现
运动功能障碍的多维表现
运动异常是苍白球病变最突出的临床特征,其表现形式因病变部位、范围及病因不同而存在显著差异,可概括为运动过少-运动过多综合征的不同组合。
运动减少型症状以动作迟缓、运动幅度减小及启动困难为核心,常见于苍白球内侧段病变或功能亢进状态。患者表现为肢体活动笨拙,系鞋带、扣纽扣等精细动作完成困难,行走时步幅变小,转身缓慢,呈现典型的"小碎步"步态。在疾病早期,可能仅表现为单侧肢体活动欠灵活,随着病情进展可累及双侧。这种运动减少与苍白球过度抑制丘脑-皮层运动通路密切相关,导致大脑皮层发出的运动指令无法有效传递至外周。
运动增多型症状则包括肌张力障碍、震颤、舞蹈样动作及肌阵挛等,多见于苍白球外侧段损伤或环路调控失衡。肌张力障碍表现为持续性肌肉收缩,引起异常姿势或扭转动作,如颈部向一侧歪斜(痉挛性斜颈)、手指不自主屈曲等;舞蹈样动作则为无目的、不规则的肢体摆动,类似舞蹈样动作,常见于亨廷顿病等遗传性苍白球病变;而震颤在苍白球病变中多表现为姿势性或动作性震颤,与帕金森病的静止性震颤有所区别,其频率通常在4-7Hz。
值得注意的是,部分患者会出现运动协调障碍,表现为动作幅度控制不佳,如取物时手的摆动幅度过大(辨距不良),或肢体在运动过程中出现不规则抖动(意向性震颤)。这种协调异常可能与苍白球-小脑环路的交互作用受损有关。
非运动症状的隐匿性与复杂性
长期以来,苍白球病变的非运动症状常被忽视,但近年来研究表明,这类症状对患者生活质量的影响可能不亚于运动障碍,且涉及多个系统。
认知与情绪障碍在苍白球病变中较为常见,尤其是内侧苍白球与边缘系统存在广泛联系的病例。患者可出现执行功能下降,表现为计划、组织及问题解决能力减退,难以完成多步骤任务;记忆力减退以工作记忆受损为主,对近期发生的事情遗忘明显;部分患者会出现类似抑郁的表现,如情绪低落、兴趣减退、快感缺失,这可能与苍白球-边缘叶环路的多巴胺能神经支配异常有关。而在肝豆状核变性等疾病中,患者还可能出现人格改变,如易怒、冲动控制障碍。
自主神经功能紊乱在某些苍白球病变中也可出现,表现为血压波动(直立性低血压较为常见)、出汗异常(多汗或无汗)及排尿功能障碍等。这种自主神经异常可能与苍白球通过下丘脑对自主神经中枢的调控失衡有关,在晚期帕金森叠加综合征患者中更为明显。
语言与吞咽功能障碍主要见于病变累及双侧苍白球或合并其他基底神经节结构损害的情况。患者语言变得单调、语速减慢、音量降低(小写症),严重时可出现构音障碍,吐字不清;吞咽功能受累时,表现为进食缓慢、饮水呛咳,存在误吸风险,这与咽喉部肌肉协调运动障碍相关。
不同病因所致症状的特征性差异
由于苍白球病变病因多样,不同疾病所致的症状组合具有一定特征性,掌握这些差异对临床诊断具有重要价值。
肝豆状核变性作为最常见的可治疗性遗传性苍白球病变,其症状具有"多样性"与"波动性"特点。除典型的肢体震颤、肌张力增高外,约40%-50%的患者会出现Kayser-Fleischer环(角膜缘铜沉积),这是重要的诊断线索;肝功能异常与精神症状(如幻觉、妄想)也较为常见,且症状可因治疗不及时而进行性加重。
亨廷顿病以舞蹈样动作、认知衰退及精神症状三联征为典型表现,早期多以隐匿性的肢体不协调或情绪改变起病,随病情进展舞蹈样动作逐渐明显,可波及面部、躯干及四肢,同时出现记忆力下降、判断力减退,最终发展为痴呆。该病具有常染色体显性遗传特点,家族史对诊断至关重要。
一氧化碳中毒性苍白球病变多在急性中毒后2-60天出现"假愈期",随后突然出现锥体外系症状,表现为肌张力增高、动作迟缓、表情呆板,类似帕金森病,但震颤相对少见,且常伴有不同程度的认知障碍,头部MRI可见双侧苍白球对称性长T1、长T2信号。
药源性苍白球损害常见于长期服用抗精神病药物(如氟哌啶醇、氯丙嗪)的患者,表现为急性或亚急性起病的肌张力障碍(如颈后仰、舌外伸)、类帕金森综合征(运动迟缓、肌强直),部分患者可出现口-舌-颊三联征(不自主伸舌、咀嚼动作),停药或减药后症状多可缓解。
大脑苍白球病变吃什么药?
对症治疗药物:改善运动症状的核心选择
针对苍白球病变所致的运动功能障碍,药物治疗的主要目标是调节基底神经节环路的神经递质平衡,根据症状类型不同,选择的药物类别及作用机制存在差异。
抗胆碱能药物主要用于缓解肌张力增高及震颤症状,其代表药物为苯海拉明、苯扎托品,通过阻断中枢M胆碱受体,减弱乙酰胆碱的作用,恢复多巴胺与乙酰胆碱的递质平衡。这类药物对震颤的改善效果优于肌强直,尤其适用于年轻患者,但老年患者需慎用,因其可能引发认知功能下降、口干、便秘等副作用。临床研究显示,苯海拉明在治疗药源性肌张力障碍时,有效率可达60%-70%,通常采用口服给药,起始剂量25mg/次,每日2-3次,可根据反应逐渐调整剂量。
多巴胺能药物包括左旋多巴及其复方制剂(如美多芭、息宁)、多巴胺受体激动剂(普拉克索、罗匹尼罗),主要用于改善运动迟缓及肌强直。左旋多巴作为多巴胺前体,进入脑内后转化为多巴胺,补充苍白球病变导致的多巴胺能神经传递不足,对帕金森样症状效果显著。研究表明,左旋多巴可使约70%的苍白球病变患者运动症状得到改善,但长期使用可能出现疗效减退及运动并发症(异动症、开关现象)。多巴胺受体激动剂则直接刺激多巴胺受体,作用较左旋多巴温和,适用于早期患者或作为左旋多巴的辅助用药,普拉克索的常用起始剂量为0.125mg/次,每日3次,可逐渐增至0.5mg/次。
GABA能药物如氯硝西泮、巴氯芬,通过增强γ-氨基丁酸的抑制作用,缓解肌张力障碍及肌阵挛。氯硝西泮对肌阵挛的疗效较为肯定,口服起始剂量0.5mg/晚,可逐渐增至2-4mg/日,分2-3次服用,但需注意嗜睡、共济失调等副作用;巴氯芬主要用于脊髓水平的肌张力增高,但对某些苍白球病变所致的肢体肌张力障碍也有一定效果,通常从小剂量5mg/次开始,每日3次,可逐步增加至10-15mg/次。
病因针对性治疗:从源头干预的关键药物
对于明确病因的苍白球病变,除对症治疗外,针对病因的特异性药物治疗是改善预后的关键,尤其是遗传性或代谢性疾病。
肝豆状核变性的治疗以驱铜与阻止铜吸收为主,青霉胺是最经典的驱铜药物,通过与铜离子结合形成可溶性复合物排出体外,推荐剂量为20-30mg/(kg·d),分3-4次口服,用药期间需定期监测血常规及肝肾功能;曲恩汀(Trientine)作为二线驱铜药,适用于不能耐受青霉胺的患者,剂量为0.25-0.5g/次,每日2-3次。同时需服用锌剂(如醋酸锌)阻止肠道铜吸收,锌剂与驱铜药需间隔2小时服用,避免相互作用。研究表明,早期规范驱铜治疗可使80%以上的肝豆状核变性患者病情得到控制,显著改善苍白球病变所致的神经症状。
神经铁沉积性疾病中,对于泛酸激酶相关神经变性病(PKAN),目前尚无特效药物,但有研究显示,大剂量维生素E(800-1200IU/日)可能具有一定的神经保护作用,其机制与抗氧化应激有关,但临床疗效仍需更多研究证实。对于出现严重肌张力障碍的患者,可尝试使用肉毒毒素局部注射,缓解局部肌肉痉挛,每次注射剂量根据受累肌肉大小调整,通常每3-6个月注射一次。
感染或免疫介导的苍白球病变如病毒性脑炎累及苍白球时,需根据病原体选择抗病毒药物(如阿昔洛韦用于单纯疱疹病毒感染,剂量为10mg/kg,每8小时一次,静脉滴注),同时可短期使用糖皮质激素(如甲泼尼龙1g/日,冲击治疗3-5天)减轻炎症反应及脑水肿。对于自身免疫性基底神经节脑炎,可采用免疫球蛋白(0.4g/kg·d,静脉滴注5天)或血浆置换治疗,部分患者需联合免疫抑制剂(如环磷酰胺)预防复发。
并发症管理与支持治疗药物
苍白球病变除运动及非运动症状外,常伴随多种并发症,合理使用相关药物可显著改善患者生活质量,减少不良反应。
认知与情绪障碍的药物干预:对于出现抑郁症状的患者,可选用选择性5-羟色胺再摄取抑制剂(SSRI)如舍曲林(起始剂量50mg/日,可增至100-150mg/日)或氟西汀(20-40mg/日),这类药物对运动症状影响较小;若合并焦虑,可短期使用苯二氮䓬类药物(如阿普唑仑0.4mg/次,每日2-3次),但需注意过度镇静及依赖性。对于认知功能下降明显的患者,可尝试使用胆碱酯酶抑制剂如多奈哌齐(5-10mg/日),可能对轻度认知障碍有一定改善作用,但对中重度痴呆效果有限。
自主神经功能紊乱的药物治疗:直立性低血压是常见的自主神经症状,可选用氟氢可的松(0.1-0.3mg/日)增加血容量,或米多君(2.5-10mg/次,每日3次)收缩血管,提升血压;出汗异常可使用抗胆碱能药物如溴丙胺太林(15-30mg/次,每日3次)缓解多汗症状,但需注意口干、便秘等副作用。排尿功能障碍表现为尿频、尿急时,可选用托特罗定(2mg/次,每日2次)或索利那新(5-10mg/日)阻断膀胱M受体,改善症状。
药物副作用的防治:长期使用抗帕金森药物可能出现恶心、呕吐等胃肠道反应,可在服药时同时服用多潘立酮(10mg/次,每日3次)促进胃肠蠕动;出现异动症时,可减少左旋多巴剂量或加用金刚烷胺(100mg/次,每日2次)缓解不自主运动;使用青霉胺驱铜时,约10%-30%的患者会出现过敏反应,需先进行皮试,用药期间密切观察皮疹、发热等症状,必要时停药并给予抗过敏治疗。
大脑苍白球病变常见问题答疑
苍白球病变能彻底治愈吗?
苍白球病变的预后与病因密切相关。对于获得性因素如一氧化碳中毒、药源性损伤,若能早期诊断并及时去除病因,部分患者的症状可显著改善甚至基本恢复正常。而遗传性疾病如肝豆状核变性,早期规范驱铜治疗可有效控制病情进展,阻止神经损伤加重,但已形成的神经元损害多为不可逆;亨廷顿病等神经退行性疾病目前尚无根治方法,药物治疗主要是改善症状,延缓疾病进展。总体而言,能否治愈取决于病因类型、病变严重程度及治疗干预的时机。
如何早期发现苍白球病变?
早期识别苍白球病变的关键在于关注非特异性症状。当出现不明原因的肢体活动欠灵活、精细动作笨拙,或反复出现肌张力障碍(如颈部歪斜、手指痉挛),尤其是合并情绪改变、记忆力下降时,应警惕苍白球病变可能。对于有肝豆状核变性家族史者,若出现不明原因的肝功能异常伴神经系统症状,需及时进行角膜K-F环检查及铜代谢相关检测(血清铜蓝蛋白、24小时尿铜)。头部MRI检查对苍白球病变具有重要诊断价值,尤其是T2加权像可显示苍白球区域的异常信号,有助于早期发现结构改变。
药物治疗需要终身服药吗?
是否需要终身服药取决于病因及病情控制情况。对于药源性或中毒性苍白球病变,在去除病因并经短期药物对症治疗后,若症状完全缓解,可在医生指导下逐渐减药直至停药;而对于遗传性疾病如肝豆状核变性,驱铜药物(青霉胺、曲恩汀)及锌剂需要终身服用,以维持体内铜代谢平衡,避免病情反复。帕金森样症状明显的患者,多巴胺能药物通常需要长期服用,但可根据症状波动情况调整剂量及剂型。在服药过程中,需定期复诊,评估疗效及药物副作用,动态调整治疗方案。
日常生活中有哪些注意事项?
苍白球病变患者的日常管理应注重以下几点:①安全防护:运动障碍明显者需防跌倒,家中地面保持干燥,安装扶手;②心理支持:家属应关注患者情绪变化,鼓励参与社交活动,必要时寻求心理干预;③饮食调理:肝豆状核变性患者需低铜饮食,避免食用动物肝脏、坚果、巧克力等含铜高的食物;④康复训练:根据症状选择针对性康复措施,如运动迟缓者可进行步态训练,肌张力障碍者可接受物理治疗;⑤定期随访:监测病情进展及药物不良反应,复查头部MRI、肝肾功能等指标。
有哪些最新治疗进展?
近年来,苍白球病变的治疗在以下方面取得进展:①基因治疗:针对遗传性苍白球病变(如亨廷顿病),反义寡核苷酸(ASO)技术可特异性降低突变huntingtin蛋白的表达,已在动物模型中显示疗效,部分临床试验正在进行;②干细胞治疗:间充质干细胞移植可能通过分泌神经营养因子促进苍白球神经元修复,在帕金森病动物模型中已观察到运动功能改善;③神经调控技术:深部脑刺激(DBS)对药物难治性苍白球病变所致的肌张力障碍或帕金森症状效果显著,尤其是苍白球内侧段(GPi)刺激可有效缓解肢体僵直及运动迟缓;④精准医学:通过基因检测及分子分型,实现个体化用药,如根据肝豆状核变性患者的ATP7B基因突变类型选择更有效的驱铜方案。这些新技术为苍白球病变的治疗提供了新方向,但多数仍处于研究阶段,需进一步验证其安全性与有效性。
- 文章标题:大脑苍白球病变是什么病吃什么药?
- 更新时间:2025-05-23 14:54:41

 400-029-0925
400-029-0925