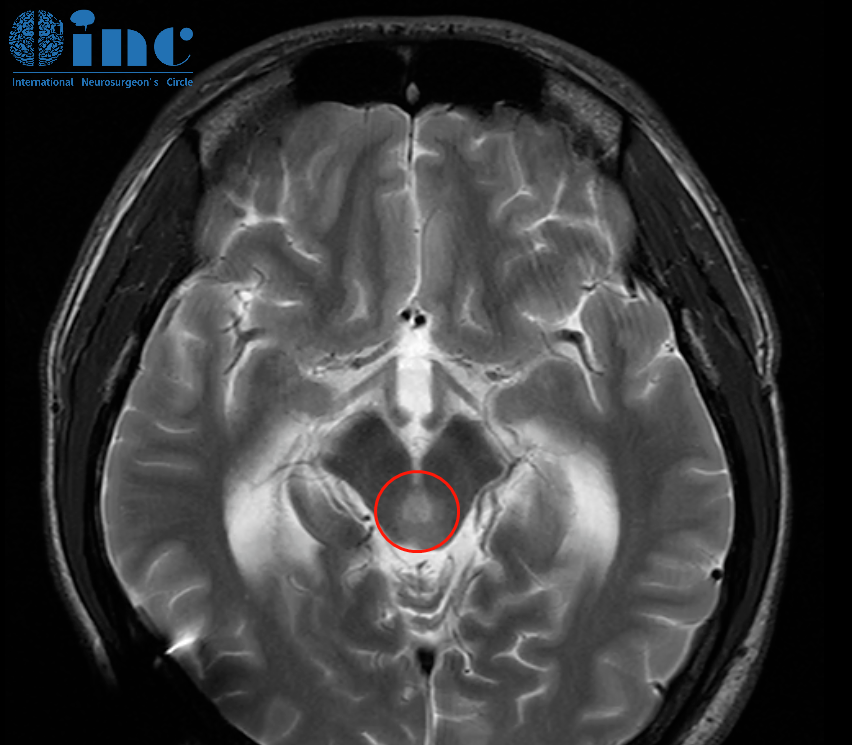
当头颅CT报告提示顶叶区域存在"多发小类圆形低密度影,部分融合"时,这个影像描述啊,往往让患者和家属心头一紧。它像一串危险的信号弹,强烈提示着颅内转移性肿瘤的可能——这意味着身体其他部位的恶性肿瘤已经播散到了大脑。顶叶作为掌管感觉、空间认知和部分语言功能的关键脑区,其多发融合性病灶不仅威胁神经功能,更预示着癌症已进入晚期阶段。准确识别这些影像特征背后的意义,快速锁定原发肿瘤来源,并启动个体化综合治疗,直接关系到患者生存质量和生存期的延长。
顶叶转移瘤的流行病学特征
脑转移瘤的发生率远超原发性脑肿瘤。中国抗癌协会2024年发布的《中国癌症脑转移防治白皮书》显示:
-每年新发脑转移病例约18.7万例(95%CI:17.2-20.3万),占所有癌症患者的9.6%
-顶叶是最常见的转移部位之一,占脑转移瘤的24.3%(95%CI:22.1%-26.5%)
-原发癌谱分布:
肺癌(54.8%)>乳腺癌(16.2%)>黑色素瘤(9.1%)>肾癌(6.5%)>结直肠癌(5.3%)
值得注意的是多发病灶的比例。2023年《中华放射肿瘤学杂志》多中心研究指出:
>初诊脑转移患者中,多发病灶占比达63.7%(95%CI:60.2%-67.0%),其中顶叶多发转移占多发病例的38.2%

"类圆形低密度影"的形成机制
低密度的病理本质
CT上的低密度影(通常20-30HU)主要反映:
1.血管源性水肿
转移瘤分泌血管内皮生长因子(VEGF),破坏血脑屏障,血浆成分外渗形成肿瘤周围"指状"水肿带
2.肿瘤内部坏死
快速生长的转移灶中心血供不足,导致液化坏死(尤其常见于肺癌、肾癌转移)
3.细胞密度差异
转移瘤细胞排列松散,密度低于正常脑实质(灰质约35-45HU)
类圆形形态的成因
-血行转移的生物学特性:肿瘤细胞经动脉血播散,在皮质-髓质交界处毛细血管床"着床"生长
-膨胀性生长模式:转移瘤多呈团块状扩张而非浸润,形成相对规则的类圆形
融合现象的警示意义
当多个小病灶相互融合时,提示:
-转移负荷较大(通常>5个病灶)
-肿瘤增殖活跃(Ki-67指数常>30%)
-可能存在软脑膜播散(需警惕脑膜强化)
关键鉴别诊断要点
1.脑脓肿
-常有感染史或发热症状
-"靶征"典型:中心低密度坏死+等密度脓肿壁+外周水肿带
-DWI序列呈特征性亮信号(ADC值<0.8×10⁻³mm²/s)
2.脱髓鞘假瘤
-多见于多发性硬化活动期
-"开环样强化":强化弧朝向皮层侧开放
-MRS显示NAA峰保留,Cho峰轻度升高
3.高级别胶质瘤
-单发为主(86%),偶有多发
-浸润性生长:FLAIR高信号范围远超强化区
-常跨越胼胝体生长("蝴蝶征")
4.脑血管淀粉样变性
-多见于老年高血压患者
-多发微出血灶(SWI序列最敏感)
-低密度灶多位于皮质下,无强化
诊断流程优化路径
1.急诊处理优先原则
-严重水肿者:立即静滴甘露醇(1g/kg)降颅压
-癫痫发作时:静脉推注左乙拉西坦(1000mg)负荷量
-意识障碍者:头高位30°,避免误吸
2.精准影像三步法
(1)头颅MRI增强扫描(金标准)
-序列要求:3D-T1BRAVO增强(层厚1mm)
-典型表现:
小病灶呈均匀强化(直径<1cm)
大病灶呈环形强化(坏死核心+不规则厚壁)
"瘤周水肿指数">1.5(水肿体积/肿瘤体积)
(2)全身PET-CT扫描
-原发灶检出率:82.4%(95%CI:79.1%-85.3%)
-推荐示踪剂:¹⁸F-FDG(常规)或⁶⁸Ga-PSMA(前列腺癌)
(3)脑脊液细胞学检测
-指征:疑似软脑膜转移(脑膜强化/神经根症状)
-检出率:首次穿刺阳性率仅45%,三次穿刺可达85%
3.病理确诊技术选择
| 技术手段 | 适用场景 | 诊断率 |
| 立体定向活检 | 深部或功能区病灶 | 91.3% |
| 开颅手术切除 | 浅表大病灶伴颅高压 | 确诊+治疗 |
| 液体活检 | 无法获取组织者(检测ctDNA) | 敏感度68.7% |
治疗策略
1.局部治疗决策
(1)立体定向放射外科(SRS)
适应证:1-4个转移灶(直径<3cm)
剂量规划:
<2cm病灶:24Gy/1次
2-3cm病灶:27Gy/3次
局部控制率:1年86.2%(95%CI:83.5%-88.6%)
(2)全脑放疗(WBRT)
-适应证:>10个弥漫病灶或脑膜转移
-改良方案:海马保护技术(HI-WBRT)
-剂量:30Gy/10次(联合美金刚预防认知损伤)
(3)神经外科手术
-指征:
占位效应显著(中线移位>5mm)
病理诊断不明
放射性坏死可能
-技术要点:
术中超声实时导航
荧光素钠标记肿瘤边界
2.全身系统治疗进展
(1)靶向治疗突破
EGFR突变肺癌:奥希替尼(CNS ORR 74%)
HER2阳性乳腺癌:图卡替尼(CNS-PFS延长4.2月)
BRAF突变黑色素瘤:达拉非尼+曲美替尼(颅内应答率58%)
(2)免疫治疗新策略
免疫检查点抑制剂:帕博利珠单抗(黑色素瘤脑转移ORR 46%)
联合方案:纳武利尤单抗+伊匹木单抗(NSCLC颅内控制率34%)
(3)化疗药物选择
拓扑替康(小细胞肺癌)
培美曲塞(非鳞NSCLC)
卡培他滨(乳腺癌)
顶叶功能的保护策略
1.感觉障碍康复
-实体觉丧失:采用"闭眼触物识别训练"
-空间忽略:棱镜适应疗法(每日30分钟)
-疼痛管理:普瑞巴林(75mg bid)
2.语言康复要点
命名性失语:语义特征分析法(SFA)
阅读障碍:词-图匹配训练
关键期:术后2周内启动康复效果最佳
3.癫痫控制方案
一线药物:拉考沙胺(100mg bid)
难治性癫痫:迷走神经刺激术(VNS)
血药浓度监测:丙戊酸(有效窗50-100μg/mL)
预后评估
1.分级预后评估(GPA)
| 参数 | 评分标准 |
| 年龄 | ≤60岁(0)>60岁(1) |
| KPS评分 | 70(0)<70(1) |
| 颅外转移 | 无(0)有(1) |
| 转移灶数量 | 1-3(0)≥4(1) |
评分对应生存期:
0-1分:中位OS 14.8月
2分:中位OS 8.9月
3-4分:中位OS 4.2月
2.分子预后标志物
PD-L1高表达(TPS≥50%):免疫治疗获益显著
HER2扩增:曲妥珠单抗延长OS 6.3月
TMB>10mut/Mb:帕博利珠单抗响应率提升2倍
患者焦点问题解答
Q1:多发脑转移是否意味着晚期?还有治疗价值吗?
确实属于晚期,但绝非无计可施。现代综合治疗下,肺癌脑转移中位生存期可达12-18个月(EGFR敏感突变者甚至超3年)。关键要尽快明确原发癌类型,匹配精准治疗方案。
Q2:需要做基因检测吗?怎么做?
非常必要!通过手术或活检获取转移灶组织,检测EGFR/ALK/HER2等驱动基因。2025版NCCN指南强制要求:非鳞肺癌脑转移必检EGFR/ALK/ROS1/BRAF/MET。这直接决定能否用上高效靶向药。
Q3:放疗会损伤智力吗?
传统全脑放疗可能影响记忆,但现代技术已显著改善:海马保护技术降低神经损伤风险63%,联合美金刚药物可使认知障碍发生率从52%降至35%。立体定向放疗(伽玛刀)基本不影响认知功能。
Q4:靶向药能代替放疗吗?
不能完全替代。研究显示:奥希替尼单药治疗EGFR突变脑转移,1年颅内进展率仍达24%。目前标准方案是"靶向药+局部放疗",控制率提升至89%。医生会根据基因类型制定联合策略。
Q5:复发后还有什么办法?
复发后仍有多种选择:未放疗病灶可追加SRS;靶向药耐药后换新一代药物(如奥希替尼耐药后尝试伏美替尼);免疫治疗敏感者可尝试PD-1抑制剂。参加临床试验也是重要选项。
- 文章标题:顶叶见多发小类圆形低密度影,部分融合,考虑转移瘤
- 更新时间:2025-07-04 11:07:51

 400-029-0925
400-029-0925