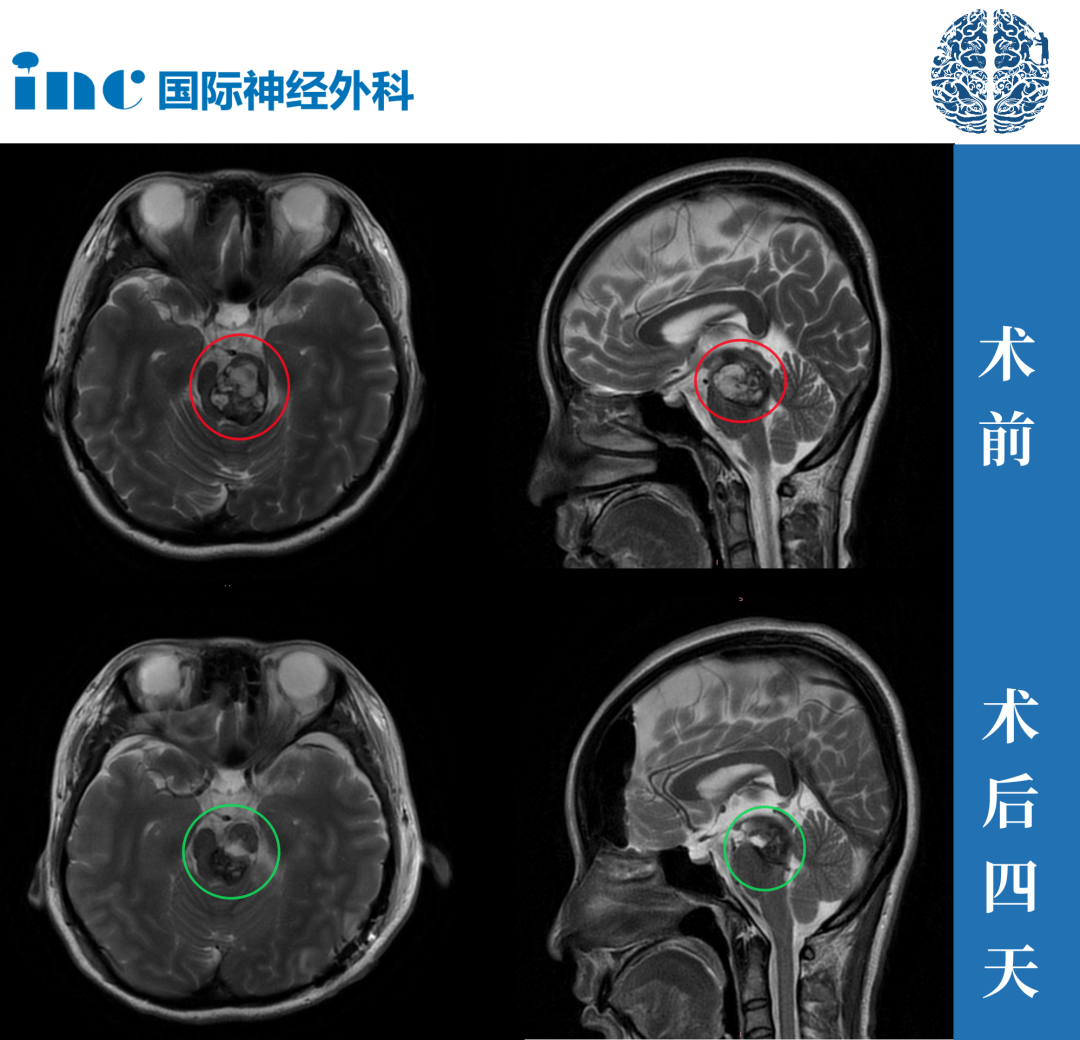
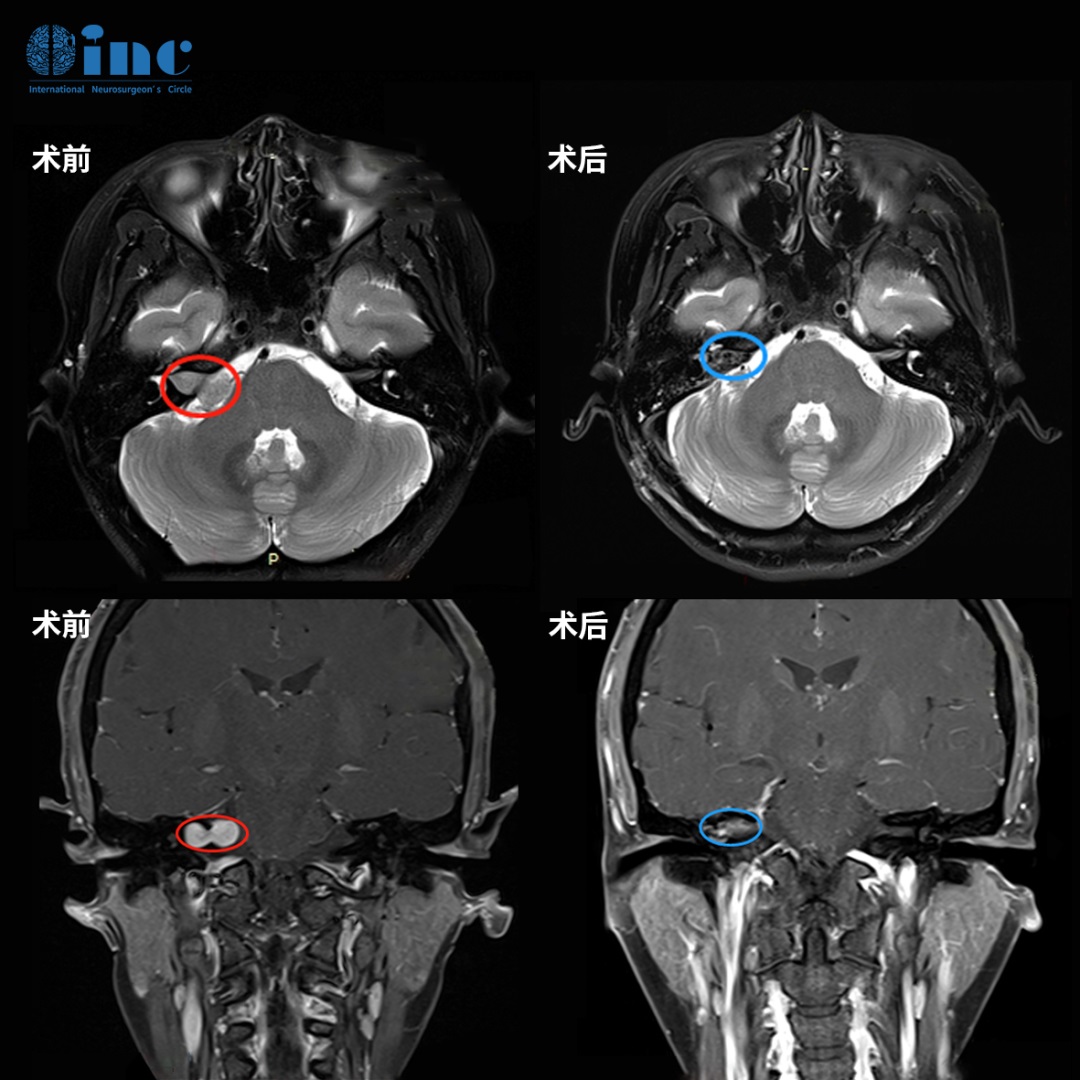
脑胶质瘤是较常见的脑部原发性肿瘤,占全部原发肿瘤的28%和脑部恶性肿瘤的80%。神经胶质瘤起源于神经胶质干细胞或祖细胞,具有很强的攻击性。WHO按其恶性程度分为Ⅰ~Ⅳ级。...
脑胶质瘤是较常见的脑部原发性肿瘤,占全部原发肿瘤的28%和脑部恶性肿瘤的80%。神经胶质瘤起源于神经胶质干细胞或祖细胞,具有很强的攻击性。WHO按其恶性程度分为Ⅰ~Ⅳ级。
胶质母细胞瘤是弥漫性神经胶质瘤的一种高级形式,其特点为弥漫性浸润.是成人较常见的中枢神经系统恶性肿瘤,约占46.6%。成年患者GBM发病率随年龄升高而升高,诊断中位年龄为64岁。
一旦确诊后不能完全痊愈,即使手术全切除及术后规律性放疗,其中位总生存期也不过14个月左右,5年存活率仅为5.5%。近几年来研究发现,化疗药物治疗恶性胶质瘤有疗效。
TMZ主要通过促进胶质瘤细胞的DNA甲基化来发挥作用。但是多种DNA修复机制可修复TMZ所致DNA损伤,包括肿瘤细胞O6-甲基鸟苷DNA甲基转移酶,碱基切除修复MMR等,在神经胶质瘤耐药性TMZ中起重要作用。另外,自噬是一种蛋白质降解途径,依赖于溶酶体,还与TMZ的耐药性有复杂的关系。
现在已经有一些针对上述机制的药物在提高耐药能力方面发挥了作用,但对延长GBM患者的生存期没有作用。该文主要针对近年来有关胶质瘤对TMZ耐药的DNA修复机制及TMZ抗TMZ的研究进展作一综述。
自噬是一种细胞通过溶酶体途径降解受损细胞器,以及错误折叠、功能不正常的蛋白质,从而为细胞提供能量的机制。细胞与组织的自噬平衡,以及代谢.发育.免疫,病原菌清除等方面都扮演着重要的角色。日益增多的研究显示,自噬作用在肿瘤形成过程中具有重要作用。自噬具有促进或控制肿瘤的双重作用,与肿瘤的类型和背景有关。其一,通过去除非折叠蛋白和无用的细胞器,自噬能控制肿瘤的发生。反之,在生理或压力条件下,可将无用的蛋白质分解成细胞核。
提示:本文内容来自网络用户投稿,仅供参考,不做为诊断依据,任何关于疾病的建议都不能替代执业医师的诊断。请以医生诊断为准,不代表本站同意其说法,请谨慎参阅,本站不承担由此引起的任何法律责任。
- 文章标题:胶质瘤耐药性DNA修复和自噬作用机制研究进展
- 更新时间:2023-03-26 22:56:38
-
前颅窝底占位不一定就是胶质瘤。前颅窝底占位性病变并不等同于胶质瘤。这个区域的占...
2026-01-27 11:21:41
-
胶质母细胞瘤靶向治疗是什么意思?胶质母细胞瘤是中枢神经系统最常见的恶性肿瘤,占...
2026-01-13 13:38:57
-
胶质瘤靶向治疗是什么意思?胶质瘤靶向治疗,是指在细胞分子水平上,针对胶质瘤细胞...
2026-01-12 17:44:13
-
胶质瘤保守治疗是什么意思?胶质瘤保守治疗,简单来说,是指在不进行开颅手术的情况...
2026-01-12 17:25:24
-
胶质母细胞瘤患者五年生存率从5%提高到13%,国产电场治疗设备的问世让这项创新技术更...
2026-01-12 16:36:30
-
如何切除脑干胶质瘤 脑干胶质瘤是神经外科医生的一个沉重话题,大部分都是恶性的。...
2023-04-25 15:25:31
-
小脑半球胶质瘤4厘米能手术吗?小脑半球胶质瘤4厘米是否能手术需要综合考虑解剖学因素...
2024-12-25 14:26:53
-
脑干胶质瘤是一种位于脑干的肿瘤,常见的症状和体征包括以下几个方面: 1. 神经系统...
2023-06-30 15:03:49
-
脑干胶质瘤的治疗方法 脑干胶质瘤患者,可选择以下几种方法进行治疗: 放射治疗 目前...
2023-04-11 10:20:19
-
脑干胶质瘤可以进行手术治疗,但是否适合手术和手术费用因多个因素而异。 首先,适...
2023-06-29 11:55:30
-
恶性肿瘤是一种严重的疾病,其中弥漫性胶质瘤就是其中之一。这种肿瘤主要发生在中枢...
2024-05-24 15:22:03
-
桥小脑角区胶质瘤二次手术可能面临一些危险和挑战。桥小脑角区位于脑部的复杂区域,...
2024-04-11 17:33:02
-
脑室胶质瘤的治疗 目前,脑室胶质瘤的治疗方法主要包括手术、放疗、化疗等。对于胶...
2022-11-09 13:49:58
-
岛叶胶质瘤手术要多少钱 岛叶胶质瘤通常需要手术切除,根据术后病理阶段,有些患者还需...
2023-03-10 11:34:22
-
脑干胶质瘤是一种恶性肿瘤,治愈率较低。然而,治疗的目标是控制疾病的进展、缓解症...
2023-06-30 17:50:04
-
脑干胶质瘤怎么检查出来 磁共振成像(MRI) 磁共振成像(MRI)检查是诊断脑干胶质瘤的优选辅...
2023-05-25 15:20:12
-
大脑脚胶质瘤是一种具有挑战性的脑肿瘤,其预后不确定。患者的生存期长短取决于多个...
2024-03-26 16:37:23
-
脑干胶质瘤后期症状 脑干胶质瘤的晚期症状可分为三个阶段:一是血管损伤,出现头痛、...
2023-04-23 16:48:08
-
治疗视神经胶质瘤较好的医院目前没有机构进行,国内治疗视神经胶质瘤的医院有很多,...
2024-07-27 18:10:29
-
脑干胶质瘤后期会有出血情况吗 脑干胶质瘤后期可能会有流血状况。脑干出血一般是由...
2023-04-21 14:10:47
-
恶性胶质瘤是什么? 恶性胶质瘤,多数属于恶性肿瘤,是侵袭性生长,手术不易切割,...
2022-03-23 12:36:43
-
脑干胶质瘤三级手术能成功吗?成功后能存活几年?脑干胶质瘤是一种位于脑干区域的恶性...
2024-08-29 16:17:44
-
高级别胶质瘤能活多久(生存期)? 高级胶质瘤患者能活多久与许多因素有关。一般来...
2022-06-10 10:44:56
-
中脑导水管胶质瘤严重吗?中脑导水管胶质瘤是一种发生在中脑导水管区域的脑肿瘤,其...
2024-04-16 18:53:10
-
脑干胶质瘤术后复发率受到多种因素的综合影响,包括肿瘤病理类型、切除程度、辅助治...
2025-03-25 19:06:15


 400-029-0925
400-029-0925