(胶质瘤)miRNA与胶质瘤微环境,随着肿瘤研究的深入,科学界逐渐意识到对肿瘤的认识不应只局限于肿瘤细胞本身,肿瘤所处的微环境也对肿瘤的恶性生物学行为具有重要的影响。对...
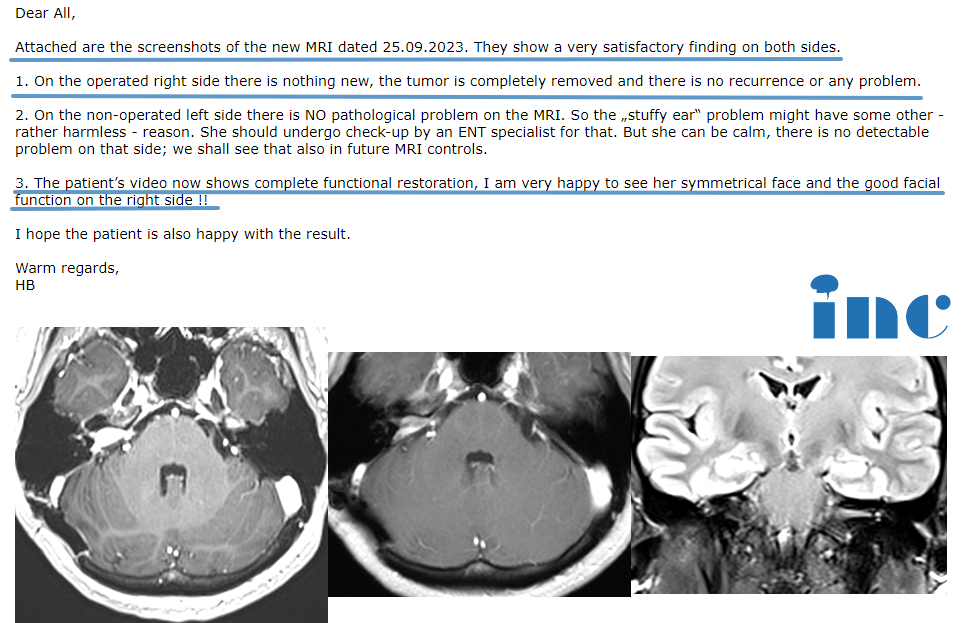
(胶质瘤)miRNA与胶质瘤微环境,随着肿瘤研究的深入,科学界逐渐意识到对肿瘤的认识不应只局限于肿瘤细胞本身,肿瘤所处的微环境也对肿瘤的恶性生物学行为具有重要的影响。对胶质瘤而言,肿瘤微环境的特点又可以从两个角度去分析,一个角度是其复杂的细胞组成,包括内皮细胞、巨噬细胞、小胶质细胞;另一个角度是其独特的理化特性,例如低氧、低pH值等。胶质瘤同所处微环境之间常通过外泌体、囊泡中包含的miRNA进行交流。
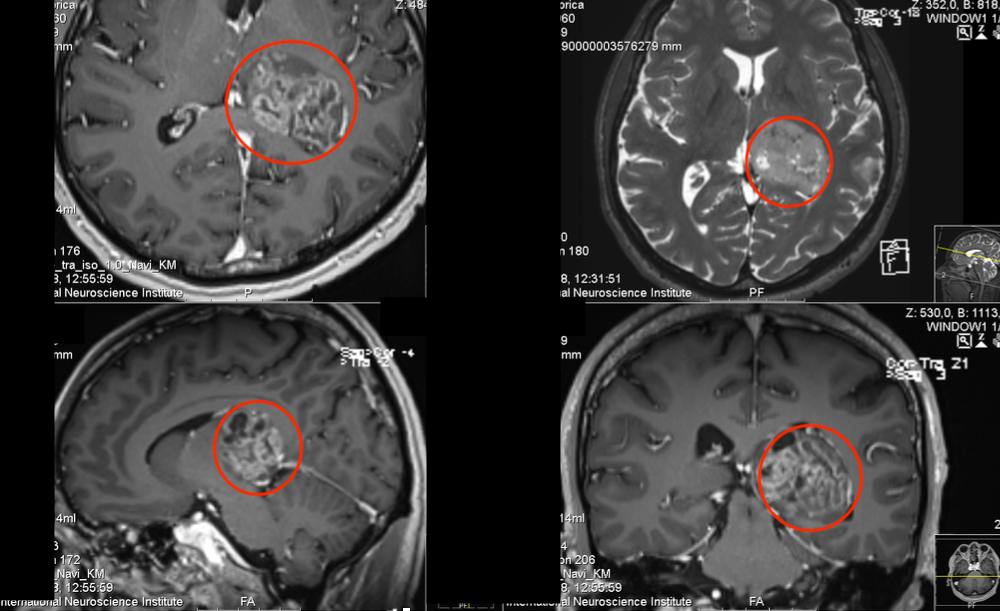
不同胶质瘤微环境之间的差异,可以导致截然不同的肿瘤特点,其中就包括对化疗药物的敏感度。既往研究发现,丰富的血供是高级别胶质瘤的普遍特点,而且胶质瘤供血血管的内皮细胞相对正常脑血管而言,具有细胞核大、胞质多、核仁多等不同表型。高级别胶质瘤来源的血管内皮细胞也表现出对化疗的不敏感,原因可能与细胞内抗凋亡基因的激活和着丝粒异常有关。miR-9在胶质瘤标本与细胞系中存在过高表达的特点。
进一步研究发现,血管内皮细胞可以吸收来自胶质瘤外泌体中的miR-9,增强血管新生的能力。与之相反,胶质瘤细胞内过高表达的miR-107在细胞共培养实验中,会控制人脑微血管内皮细胞的增殖、迁移等过程以及血管新生关键因子血管内皮生长因子的表达。由此可见,miRNA对胶质瘤血管新生能力的调控可能会间接影响胶质瘤对化疗的敏感度。肿瘤相关巨噬细胞是胶质瘤微环境中的另一类重要细胞成分。根据免疫表型的不同,肿瘤相关巨噬细胞分为M1较化亚型和M2较化亚型。
在脑内存在胶质瘤时,血液中的巨噬细胞与脑实质中的小胶质细胞会向脑胶质瘤周围的微环境迁徙形成M2较化亚型的肿瘤相关巨噬细胞,诱导T细胞活化,分泌细胞外基质组成成分并刺激新生血管形成。通过分泌不同的细胞因子,如MFG-E8、IL-6等,肿瘤相关巨噬细胞还可以诱导包括胶质瘤干细胞在内的肿瘤细胞化疗敏感度下降。而在肿瘤相关巨噬细胞的形成过程中,一系列miRNA承担着重要的上游调控作用。
在与胶质瘤细胞共培养的条件下,以重要抑癌基因PTEN为靶基因的miR-32可促进血液单核巨噬细胞向M2型巨噬细胞转化,继而增强胶质瘤细胞的增殖与侵袭能力。miR-21、miR-451、miR-146-5p亦能以不同的途径介导M1型小胶质细胞向M2型巨噬细胞的转化。除上述细胞外,胶质瘤微环境不同的理化性质,如低氧、低pH值,也可在程度调控胶质瘤的化疗敏感度。
低氧微环境中,胶质瘤细胞内凋亡相关通路活性下降,造成细胞抗凋亡能力增强,有助于肿瘤适应化疗药物的细胞毒性作用等不利因素。例如低氧诱导下胶质母细胞瘤内miR-26a的高表达介导Bcl-2相关X蛋白(Bax)/Bcl-2相关细胞死亡因子(Bad)途径实现线粒体凋亡活动的控制,降低替莫唑胺的细胞毒作用。
低氧还可诱导胶质瘤细胞膜表面钙激活钾离子通道的开放,增强胶质瘤细胞的侵袭能力和化疗耐药性。此外,低氧微环境还可刺激胶质瘤以外泌体为载体释放miR-21和miR-10a,干扰机体对肿瘤的免疫机制。伴随低氧造成的应激状态,肿瘤细胞常出现无氧酵解活动,造成细胞内部及周围pH值降低。pH值下降转而又可增强P-糖蛋白通道的泵活性,降低肿瘤细胞对化疗的敏感度。
提示:本文内容来自网络用户投稿,仅供参考,不做为诊断依据,任何关于疾病的建议都不能替代执业医师的诊断。请以医生诊断为准,不代表本站同意其说法,请谨慎参阅,本站不承担由此引起的任何法律责任。
- 文章标题:(胶质瘤)miRNA与胶质瘤微环境
- 更新时间:2021-11-09 16:36:43
-
垂体瘤左侧海绵窦区残留是什么意思?手术很成功,但医生却说肿瘤有残留。这五个字背...
2026-02-09 14:36:45
-
鞍区占位性海绵窦血管瘤是什么意思?严重吗?手术室里,无影灯下,医生们正凝神屏息...
2026-02-09 14:02:12
-
鞍区右侧海绵窦垂体腺瘤严重吗?怎么办?临床上,垂体腺瘤一旦侵犯海绵窦,治疗难度...
2026-02-09 13:46:35
-
鞍区软骨肉瘤会引起海绵窦受累吗?颅底深处看似不起眼的肿瘤,却能通过精确的解剖路...
2026-02-09 11:57:34
-
颞下窝神经血管瘤严重吗?有哪些症状?颞下窝这个颅底深处的交通要道,一旦被神经血...
2026-02-06 14:05:55
-
脊髓肿瘤术后注意事项?脊髓肿瘤术后是一个关键的阶段,患者需要遵循一系列的注意事...
2023-08-30 16:41:51
-
小脑海绵状血管瘤是一种常见的脑血管疾病,需要进行手术治疗。小脑海绵状血管瘤费用...
2024-02-05 10:14:43
-
脑干胶质瘤放疗后还能做手术吗? 脑干胶质瘤放疗后能否做手术取决于患者的病情。一...
2022-08-31 16:22:51
-
幕上室管膜瘤三级融合什么意思?幕上室管膜瘤三级融合是指在幕上室管膜瘤的基因表达...
2024-01-31 17:21:30
-
脊索瘤的病理特征? 脊索瘤是一种发生在脊髓或脊神经根的肿瘤,其病理特征可以根据...
2023-07-20 11:30:56
-
脑干海绵状血管瘤生孩子会脑出血吗?对于患有脑干海绵状血管瘤的女性患者来说,生孩...
2024-10-22 18:57:46
-
脑干毛细胞型星形细胞瘤是一种少见的脑部肿瘤,通常发生在脑干区域。在医学上,它被...
2024-04-09 15:02:18
-
颅底肿瘤切除术是一种的手术,属于四级手术。在手术级别中,一级手术是指简单的门诊...
2024-06-19 11:48:44
-
延髓桥脑胶质瘤是一种少见且具有挑战性的脑肿瘤。对于患者的预后和生存期,由于多种...
2024-03-20 13:31:33
-
脑干海绵状血管瘤是一种少见而的疾病,其手术治疗需要由的神经外科医生来执行。选择...
2024-01-03 14:35:52
-
脑海绵状血管瘤是一种血管发育异常所导致的病变,其具体形成原因尚不完全清楚。然而...
2023-06-26 16:03:33
-
脊索瘤手术后会复发吗能活多久啊?脊索瘤手术后是否会复发和患者的预后情况取决于多...
2023-07-06 16:24:03
-
颅内海绵状血管瘤出血能吸收吗?颅内海绵状血管瘤是一种少见的颅内肿瘤,出血是其常...
2023-11-03 17:50:45
-
左侧丘脑胶质瘤是一种位于大脑左侧丘脑区域的良性或恶性肿瘤。它的症状可能会因肿瘤...
2023-06-28 16:41:28
-
海绵状血管瘤做完手术会复发吗 海绵状血管瘤做完手术会复发的概率小。 只要是属于单...
2022-10-12 23:30:28
-
脑干肿瘤复发还能活多久? 脑干肿瘤复发如果是恶性肿瘤可能只有几个月生存期,如果...
2022-08-23 16:47:11
-
蝶骨嵴脑膜瘤病理诊断 1.视神经鞘脑膜瘤的四联征侧性眼凸,视力丧失,慢性浮肿性视盘...
2023-04-20 16:10:06
-
垂体瘤微创手术多久恢复?需要注意什么?垂体瘤微创手术是一种用于治疗垂体瘤的手术方...
2024-05-22 17:03:27
-
右侧颞叶脑膜瘤手术难度较大,因为该部位毗邻重要的神经和血管,手术过程中需要特别...
2024-05-14 15:11:45
-
一级星形细胞瘤术后能活多久? 星形细胞瘤一级不能活一辈子,因人而异。要看个人体...
2023-03-06 16:36:23


 400-029-0925
400-029-0925