IL-13Rα2嵌合抗原受体T细胞细胞。
IL-13Rα2的表达与胶质瘤级别呈正相关,70%以上胶质母细胞瘤表达过度,而在正常脑组织中几乎没有表达。高效表达IL-13Rα2并激活Src/PI3K/Akt/mTOR信号通路,促进肿瘤细胞的增殖、侵袭和转移。IL-13Rα2是IL-13受体的2个亚基之一,IL-13能与IL-13Rα1低亲合力结合,随后IL-13Rα1与IL-4Rα1形成异二聚体,激活STAT6信号通路,诱导细胞凋亡。IL-13Rα2与IL-13具有高度亲和性,是一种诱饵受体,可作为肿瘤细胞凋亡逃逸的机制。
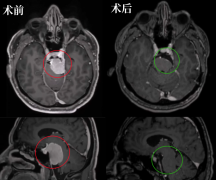
2015,Brown等共3例患者术后经瘤腔内靶向IL-13Rα2的嵌合抗原受体T细胞治疗复发性胶质母细胞瘤,存活时间较高为14个月,其中2例为客观影像学表现,发生的不良事件,如头痛和暂时性神经功能缺损,一代IL-13Rα2嵌合抗原受体T细胞在人体内存活时间14d,缺少持续性。
Brown等在前期研究的基础上,于2018年完成了二代IL-13Rα2靶向嵌合抗原受体T细胞的研制,叫做IL-13BBθT,它可以减少脱靶细胞受体的相互作用,细胞内信号传导结构CD137(4-1BB)、在小鼠模型试验中,加入截短信号CD19(CD19t),并与嵌合抗原受体T细胞相比,IL-13BBSPT与一代嵌合抗原受体T细胞结合在一起,且具有更持久的抗肿瘤效果,虽然没有出现明显的毒性反应,但肿瘤局部给药途径似乎要好于静脉给药。
经临床研究报告,1例复发性多发性胶质母细胞瘤患者在瘤腔内连续6次输注IL-13Rα2嵌合抗原受体T细胞,输入点未见肿瘤生长,后10次脑室给药及脊髓新发瘤均为颅内肿瘤,三次脑室内给药后,头颅及脊椎肿瘤明显缩小。以18F-9-[4-氟-3-(羟甲基丁]鸟嘌呤PET分子显像研究将Keu等与CD8+毒性T淋巴细胞过继至体内,在IL-13Rα2嵌合抗原受体T细胞中,用单纯疱疹病毒1型胸苷激酶作为酶报告基因,该法能够精确监测嵌合抗原受体T细胞细胞的活性.生物分布,传输过程等。
EGFRvIII,EGFRvⅢ,EGFRvⅢ,EGFRvIII,EGFRvIII),属于EGFRvIII。
EGFR是一个酪氨酸激酶受体,在多种肿瘤中表达障碍。由于EGFRvIII缺乏结合胞外配体的结构域,因此,该突变体不依赖于配体,因而不依赖于胞外配体。能够连续地激活下游的多条信号通路(例如PI3K.Ras等),导致肿瘤细胞增殖、血管新生.侵袭等一系列反应。EGFRvⅢ在30%的胶质母细胞瘤中呈阳性表达,而在正常组织中未见表达,是治疗胶质母细胞瘤顺利可行的合适靶点。
Morgan等人利用CD28-41BB-CD3?作为三代EGFRvⅢ,利用CD28-41BB-CD3θ作为T细胞信号传导结构,可以特异地识别GSCs和胶质瘤细胞系,对正常组织细胞没有影响。EGFRvⅢ靶向性嵌合抗原受体T细胞能合适地通过胶质母细胞瘤模型小鼠的肿瘤部位,显示其抗肿瘤作用。
利用该技术,郑岩等人研制出三代EGFRvIII靶向嵌合抗原受体T细胞,具有特异性杀伤EGFRvⅢ型胶质瘤细胞。首先是O'Rourke等人进行III靶向嵌合抗原受体T细胞治疗EGFRv,共10例患者通过静脉注射EGFRvⅢ靶向嵌合抗原受体T细胞治疗复发性胶质母细胞瘤,有一部分患者有肿瘤外毒性及细胞因子释放综合征,平均生存时间8个月,1例患者生存时间在18个月以上。
大部分EGFRvⅢ型胶质母细胞瘤在复发时仍保持EGFRvⅢ型,但部分患者会发生改变,所以对于那些接受EGFRvⅢ靶向治疗的胶质母细胞瘤患者,建议重复活检,并对EGFRvⅢ状态进行评价。当前,针对EGFRvIII靶向嵌合抗原受体T细胞疗法(NCT02209376.NCT01454596)的临床试验仍在进行中。
humanepidermalgrowthfactorreceptor-2,HER2)靶向嵌合抗原受体T细胞靶点。
HER2是一种跨膜糖蛋白,属于EGFR家族,致癌HER2基因位于编码HER2蛋白的17号染色体上,可通过多种信号途径影响细胞的增殖和凋亡。HER2的表达与胶质母细胞瘤的预后密切相关,因此HER2是胶质母细胞瘤患者嵌合抗原受体T细胞治疗的另一个重要靶点。但由于CAR检测到肺上皮细胞中HER2低水平表达而导致1例转移性肠癌患者因嵌合抗原受体T细胞治疗而死亡的病例报告,其顺利问题备受关注。
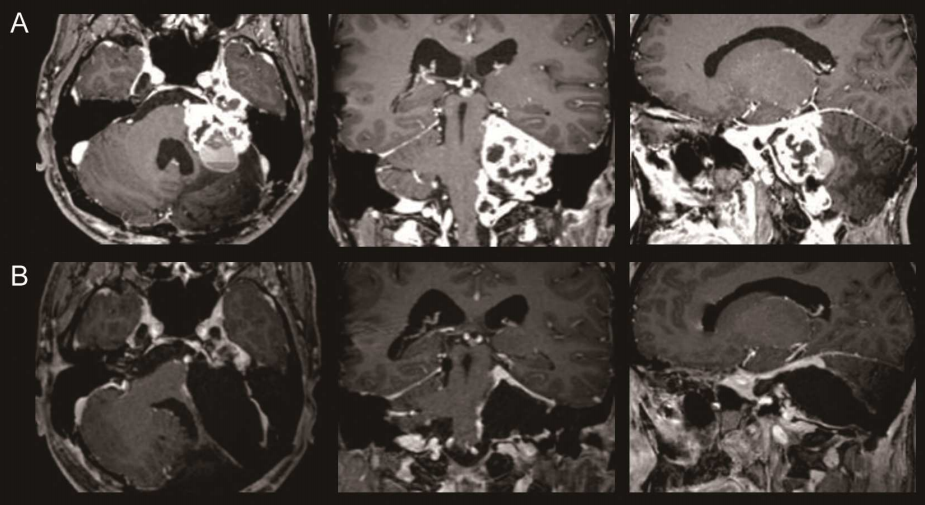
Ahmed等通过编码HER2的逆转录病毒载体,转导激活T细胞获得HER2靶向的嵌合抗原受体T细胞,发现HER2靶向嵌合抗原受体T细胞可以杀死HER2阳性胶质母细胞瘤细胞和CD133阳性干细胞,且有的抗肿瘤活性。完成了HER2靶向嵌合抗原受体T细胞(NCT01109095)的一期临床试验,全部病例均为HER2阳性或进展性胶质母细胞瘤,静脉滴注HER2靶向嵌合抗原受体T细胞,有一例局部应答超过9个月,有8-29个月无进展期,在试验中,治疗后和诊断后的中位生存期分别为11.1个月.24.5个月,未发现剂量限制毒性。2例有2级癫痫和/或头痛。
酪氨酸蛋白激酶受体2(嵌合抗原受体T细胞)。
EphA2在多种肿瘤组织中已经表达,EphA2通过Ras/ERK、PI3/Akt等途径调控细胞增殖和凋亡。EphA2表达于大多数胶质母细胞瘤,且与预后相关,因此EphA2是目前治疗胶质母细胞瘤较具吸引力的靶点。
Chow等研究发现,EphA2靶向嵌合抗原受体T细胞能诱导产生γ-干扰素和白细胞介素(interleukin),IL)-2,有明显的细胞毒作用,12只模型小鼠颅内注射2×106个EphA2靶向嵌合抗原受体T细胞后,生化荧光成像显示肿瘤信号明显减弱,在靶向嵌合抗原受体T细胞细胞数减少的情况下,小鼠生存期延长,并显示其抗肿瘤作用;但经静脉输入,未见抗肿瘤作用。
国内外已对EphA2特异性CAR进行修饰,以EphA2靶向嵌合抗原受体T细胞,其抗肿瘤活性提高20倍。针对EphA2的嵌合抗原受体T细胞(NCT0257575261)已完成了临床试验,目前还没有公布试验数据。
- 文章标题:嵌合抗原受体T细胞在胶质母细胞瘤中的具体应用
- 更新时间:2022-01-07 14:20:16

 400-029-0925
400-029-0925