James T.Rutka(鲁特卡)教授曾任世界神经外科学院院长,30多年来深耕儿童神外研究,带领团队不断突破,从脑瘤分子分型、精准治疗、新药治疗、微创治疗,为全球神经外科疑难病患儿带来希望,他发表了研究《PINK1 Is a Negative Regulator of Growth and the Warburg Effect in Glioblastoma》(PINK1是胶质母细胞瘤生长和Warburg效应的负调控因子),以下是研究简述(本篇将重点介绍研究结果及讨论)。
阅读上篇(研究设计及部分结果):【INC国际大咖研究成果】表达PINK1蛋白的胶质母细胞瘤患者生存结局更好(上)

04
PART
结果(接上篇)
PINK1过表达抑制胶质母细胞瘤细胞生长并降低ROS
为了补充我们的敲低实验,我们接下来探索了PINK1稳定表达在U87、T98G和SF188细胞中的影响。我们生成了混合的稳定PINK1-V5表位标记和空载体对照细胞系。在所有三种细胞系中,PINK1的表达在7天内显着降低了细胞增殖和细胞侵袭,PINK1稳定表达通过蛋白质印迹分析确认。PINK1表达降低了常氧下的基础HIF1A,并降低了有氧糖酵解和HIF1A反应蛋白:PDK1、HK2、LDHA和VEGFA。PDK1是HIF1A靶点,通过磷酸化PDHE1a抑制丙酮酸进入三羧酸循环。我们观察到PINK1过表达细胞中PDK1的减少导致磷酸化PDHE1a减少,支持PDK1对PDHE1a的抑制作用减弱。表达PINK1的细胞系ROS也显着降低,低氧下的细胞生长减少,并且与空载体对照细胞相比,低氧下的HIF1A蛋白表达减少。HIF1A响应低氧的关键靶基因PDK1也下调,证实了HIF1A在低氧下的活性降低。
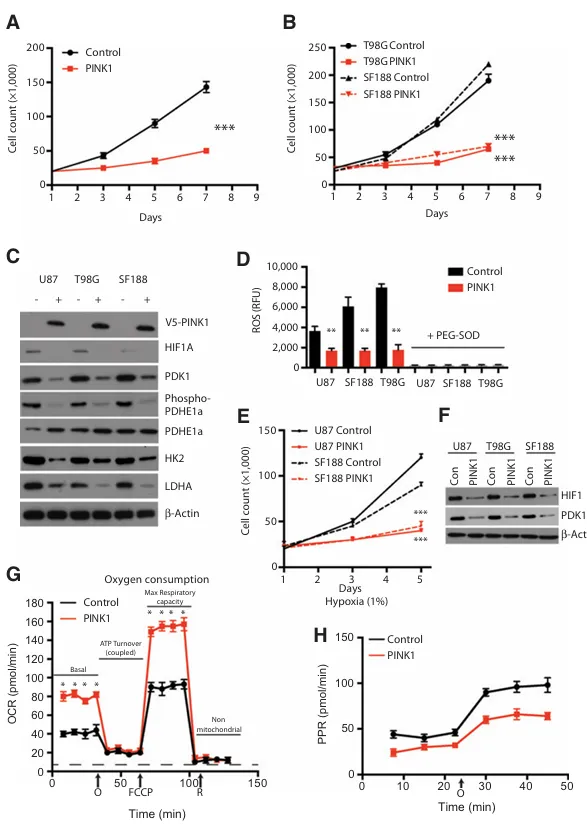
图3:PINK1过表达可阻断glioblastoma细胞生长并抑制糖酵解相关蛋白。
A,U87空载载体对照细胞与U87PINK1过表达细胞在7天内的增殖情况对比。
B,SF188和T98G空载载体对照细胞与SF188或T98GPINK1过表达细胞在7天内的增殖情况对比。
C,通过Western blot分析确认V5标记的PINK1蛋白质以及参与糖酵解和HIF1A靶标相关多种蛋白质的稳定表达情况。
D,表达空载载体对照或PINK1稳定表达状态的glioblastoma细胞中的ROS测量结果。加入100uL/mL PEG-SOD后,荧光ROS信号被淬灭。E,在低氧(1%02)条件下培养5天,比较SF188和U87空载体对照细胞与SF188或U87PINK1过表达细胞的细胞生长情况。
F,在低氧(1%O2)条件下培养72小时后,对空载体对照细胞或PINK1稳定表达细胞进行Westernblot分析,检测HIF1A及其靶基因PDK1的表达。
G,比较U87空载体对照细胞与U87PINK1过表达细胞在不同生物能量调节剂(寡霉素(0)、羰基氰化物4-(三氟甲氧基)苯踪(FCCP/F)和鱼藤酮(R))作用下的耗氧率(OCR)。箭头表示化合物添加的时间。
H、糖酵解通量分析用于测量质子生成速率(PPR,每分钟毫摩尔)。带有0的箭头表示添加寡霉素以抑制ATP合成酶,从而测量细胞的最大糖酵解能力。P<0.05;**,P<0.01;***,P<0.001
PINK1抑制胶质母细胞瘤细胞的有氧糖酵解
与PINK1敲低相反,稳定表达PINK1的U87细胞基础OCR显着增加,用FCCP处理时最大OCR增加,基础糖酵解和最大糖酵解能力通量(通过质子产生率测量)降低(图3G&H)。T98G和SF188稳定表达PINK1的细胞耗氧量也增加。所有胶质母细胞瘤细胞己糖激酶活性降低,PKM活性增加。与对照相比,稳定表达PINK1的U87、SF188和T98G在几天内测量的葡萄糖摄取和乳酸减少。
接下来,我们在原代胶质母细胞瘤培养物中表达PINK1,这些培养物在小鼠中连续传代以更好地维持胶质母细胞瘤的分子特征。在GBM8和GBM12外植体培养物中表达PINK1可减少细胞生长、侵袭、葡萄糖摄取、乳酸和己糖激酶活性。FOXO转录因子激活(包括FOXO3a)已被证明可抑制ROS和HIF1A稳定。我们假设PINK1表达可能导致FOXO3a激活。U87和T98G对照细胞均表达FOXO3a在丝氨酸294位点的抑制性磷酸化。表达PINK1的U87和T98G细胞该抑制性磷酸化位点减少,SOD2(FOXO3a的靶点)增加,SOD活性增加,支持PINK1抑制了ROS信号。通过混合siRNA敲低FOXO3a可拯救被PINK1抑制的ROS产生,我们重复实验并添加PEG-SOD以将探针氧化的变化归因于ROS。FOXO3a敲低也拯救了由PINK1表达引起的抗集落形成能力、抗细胞增殖和降低的侵袭表型。
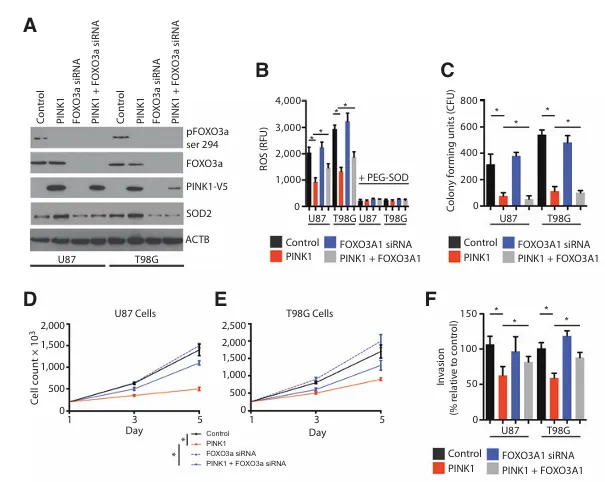
图4:PINK1能够抑制glioblastoma细胞的有氧糖酵解。
A,Western印迹分析显示,经FOXO3a聚集体siRNA处理后U87和T98G细胞与接受对照siRNA处理的细胞之间存在差异。
B,对表达对照载体或PINK1并接受FOXO3a siRNA处理的细胞进行48小时的ROS测量。荧光ROS信号经添加100/mLPEG-S0D进行淬灭。
C,集落形成试验:将500个细胞铺于6孔板中。于第10天对形成的集落进行计数。
D,U87细胞中对照载体、PINK1和FOXO3a siRNA的细胞计数情况。
E,显示了T98G细胞与对照载体、PINK1和FOXO3a siRNA的细胞计数。
F,显示了对照细胞、PINK1表达细胞和FOXO3a细胞在12小时时的侵袭实验结果。
选择性靶向表达PINK1的胶质母细胞瘤细胞导致活力降低
我们在一些胶质母细胞瘤细胞系和两个GBM癌症干细胞系中观察到PINK1表达。我们假设在这种情况下PINK1缺失会将ROS水平提升到抑制生长的水平,因为ROS也能促进抗生长效应。我们在胶质母细胞瘤癌症干细胞富集培养物G179和G144以及胶质母细胞瘤细胞系U118和U251中使用混合siRNA介导的PINK1沉默。PINK1缺失导致细胞活力降低。PINK1缺失还导致与对照细胞相比ROS水平进一步增加。胶质母细胞瘤细胞中PINK1缺失导致氧化应激增加,表现为NADP+/NADPH比率增加,谷胱甘肽耗竭,表现为GSSG水平增加和GSH:GSSG比率降低。氧化应激可以通过包括辐射在内的ROS诱导治疗使胶质母细胞瘤细胞对细胞死亡敏感。PINK1缺失使胶质母细胞瘤细胞对凋亡敏感,并在2 Gy辐射处理后减少集落形成。
PINK1在体内抑制胶质母细胞瘤生长
使用原位异种移植模型,将U87对照或PINK1过表达的U87细胞注射到免疫缺陷小鼠的额叶皮层。与对照相比,携带PINK1过表达肿瘤的小鼠中位生存时间大约延长了三倍。PINK1表达的肿瘤细胞增殖也显着减少。为了评估PINK1过表达对肿瘤负荷的影响,我们使用了表达PINK1的SF188细胞的皮下异种移植模型。过表达PINK1的SF188细胞在侧腹生长14天后的平均肿瘤重量与对照SF188细胞相比显着降低了50%。
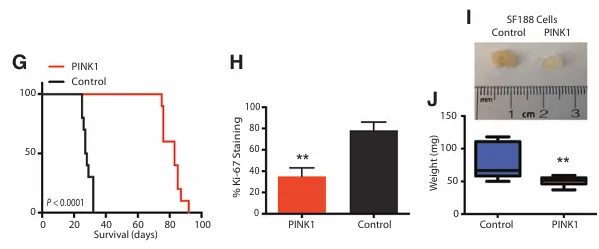
续图4:
G,显示了胶质母细胞瘤原位异种移植模型的Kaplan-Meier生存曲线分析。U87细胞(n=10)为空载体对照细胞或PINK1表达细胞(n=10)。
H,显示了图4G中Ki-67的定量分析。Ki-67的分析通过对每组5只小鼠的20个视野进行定量分析。
I,显示了将SF188对照细胞和SF188 PINK1过表达细胞移植到NOD-SCID小鼠侧腹14天后取出的肿瘤异种移植瘤的图像。
J,对NOD-SCID小鼠进行14天侧腹植入后肿瘤重量的定量分析。
肿瘤模型中的PINK1表达在进化上高度保守
为了确定其在EGFR/PI3K激活的胶质母细胞瘤发病机制中的作用,我们通过使用repo-Gal4驱动子在胶质细胞谱系中过表达果蝇直系同源基因,生成了自发性果蝇胶质母细胞瘤模型。与我们在哺乳动物细胞中的发现一致,我们发现胶质细胞特异性过表达PINK1与过表达mCherry的对照肿瘤相比,显着降低了总体肿瘤体积。我们的免疫组化分析显示,与对照相比,PINK1过表达的肿瘤表现出repo阳性胶质细胞数量显着减少。与此一致,PINK1过表达导致明显的增殖缺陷。这些发现突出了PINK1的抗肿瘤效应在远缘物种间的进化保守性,并表明其缺失可能对由生长因子受体信号通路突变激活驱动的胶质母细胞瘤的发展至关重要。
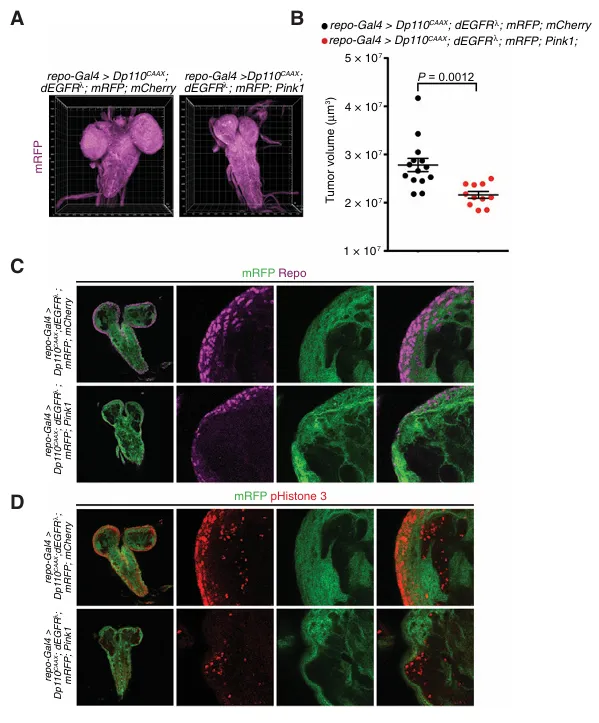
图5:Pink1在果蝇模型中的胶质母细胞瘤生长抑制作用。
A,代表性的3D堆叠共聚焦图像展示了标记为repo-Gal4驱动的mRFP表达的神经胶质组织,这些图像来自指定基因型的三龄幼虫。请注意,在相同驱动元件下Pinkl过表达显着降低了整体神经胶质肿瘤的大小。
B,体积定量结果显示,与表达mCherry的对照肿瘤相比,Pinkl过表达显着减小了神经胶质肿瘤的体积。
C,代表性的单光学切片(5umol/L)共聚焦图像显示,标记为核神经胶质标志物Repo和repo-Gal4驱动mRFP表达的肿瘤细胞数量显着减少。
D,代表性的单光学切片(5umol/L)共聚焦图像显示,标记有有丝分裂标志物磷酸化组蛋白3和由repo-Gal4驱动的mRFP表达的增殖性肿瘤细胞数量有所减少。
PINK1在脑肿瘤中下调
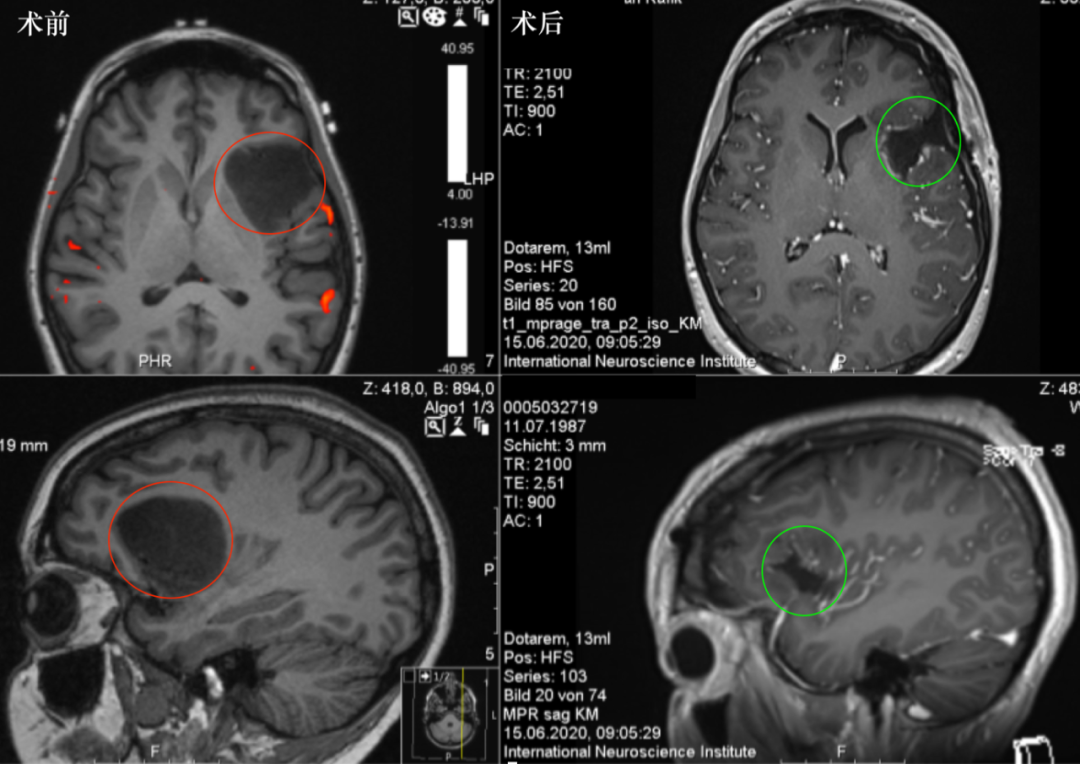
与正常脑组织相比,在REMBRANDT数据集中,2-3级胶质瘤中PINK1 mRNA表达降低,在胶质母细胞瘤中进一步降低。PINK1位于1p36号染色体,该区域在低级别胶质瘤中经常缺失。我们在TCGA低级别胶质瘤数据集中检测到103/285例低级别样本中存在PINK1杂合缺失,并且在PINK1拷贝数缺失的低级别胶质瘤中PINK1表达显着较低。GBM转录谱研究揭示该疾病包含几种分子亚型。在TCGA数据集中,PINK1表达在不同胶质母细胞瘤亚型间无显着差异。在RNA水平,PINK1表达与显着增加的无进展生存期相关,但与总生存期无关。由于PINK1蛋白稳定性的动态调节,PINK1的转录水平分析必须辅以PINK1蛋白水平表达分析。为此,我们对160多个胶质母细胞瘤肿瘤组织样本进行了免疫组化,在53%的胶质母细胞瘤样本中检测到PINK1缺失。对先前接受过替莫唑胺联合放疗的原发性胶质母细胞瘤肿瘤的组织微阵列分析显示,PINK1阴性肿瘤与较差的总生存期相关。
接下来对238个正常脑组织样本和984个原发性脑肿瘤进行了基因表达分析,以确定PINK1缺失是否在其他脑肿瘤中观察到。与位置匹配的正常脑组织相比,PINK1在包括胶质母细胞瘤在内的几种原发性脑肿瘤中显着下调。在所有四个髓母细胞瘤分子亚组中也观察到PINK1缺失。
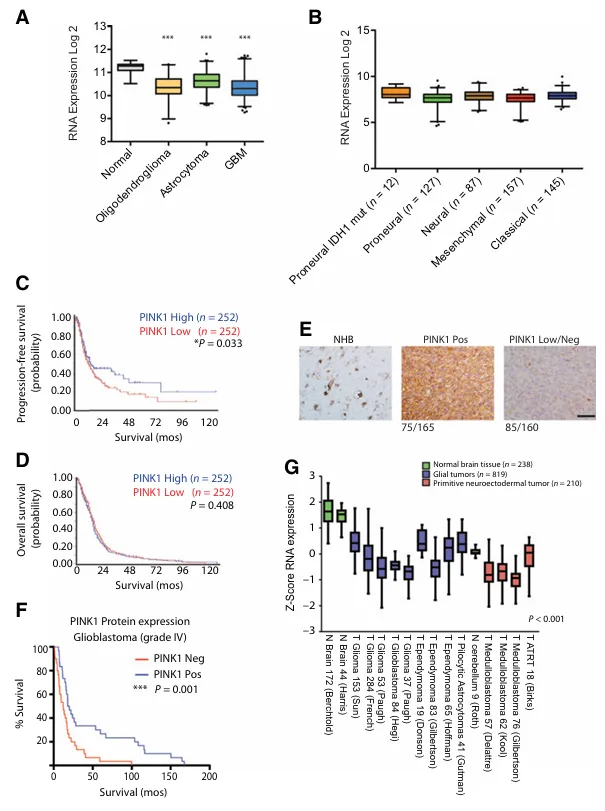
图6:PINK1在脑肿瘤中的表达水平被下调。
A,REMBRANDT数据库中PINK1基因在不同胶质瘤肿瘤样本与正常脑组织间的表达情况比较。
B,TCGA数据库中不同胶质母细胞瘤亚型中PINK1基因的表达情况(n=528)。
C,基于中位数RNA截断值计算的PINK1高基因表达与TCGA数据库中延长PFS(无进展生存期)的相关性。
D,基于中位数RNA截断值的PINK1高基因表达在TCGA数据库中并未与OS(总生存期)相关。
E,PINK1在正常脑组织与160个胶质母细胞瘤手术样本中的IHC(免疫组织化学)分析结果;标尺单位为50微米。
F,基于61例接受替莫唑胺和放射治疗的胶质母细胞瘤患者的肿瘤样本库(TMA)进行的PINK1生存分析。
G,使用R2基因组学软件进行荟萃分析,比较不同区域(包括皮层用于诊断胶质瘤、小脑用于分析超过900例原发脑肿瘤数据来自17个数据集和研究)的正常脑组织中的PINK1RNA表达情况。在所有分析的数据集中,PINK1RNA表达均显着下调。***,P<0.001。
05
PART
讨论
代谢重编程对于癌细胞产生生物量和还原力至关重要。我们证明PINK1是胶质母细胞瘤生物学的一个驱动因子,因为其缺失导致增殖增加、耗氧减少和糖酵解增加。我们的数据支持重新表达PINK1可以在体内和体外抑制胶质母细胞瘤细胞的生长。PINK1表达的减少通过升高ROS导致HIF1A稳定。癌细胞通过Warburg效应增加有氧糖酵解,并通过ROS产生更高水平的氧化应激。ROS的产生、积累和消除必须在癌细胞中受到严格调控以防止细胞死亡。ROS产生和消除的不平衡可以改变正常细胞和肿瘤细胞的表型。NHA中PINK1的缺失增加了ROS水平,并通过稳定HIF1A促进有氧糖酵解。PINK1缺失已被证明可稳定小鼠神经元和小鼠成纤维细胞中的HIF1A以维持增殖。斑马鱼中Pink1缺失已被证明可激活HIF1A靶基因;然而,未评估HIF1A蛋白表达和对有氧糖酵解的影响。我们的研究揭示了Pink1如何在癌细胞中调节HIF1A水平,促进葡萄糖摄取和利用以驱动肿瘤生长。
胶质母细胞瘤细胞中PINK1过表达减少了ROS产生,并可能抑制ROS驱动的表型,包括有氧糖酵解和增殖。这些结果与先前的研究一致,即较低水平的ROS清除酶可以促进正常细胞和癌细胞中的有氧糖酵解和代谢重编程,而过表达则减少癌细胞生长。我们观察到PINK1过表达通过FOXO3a抑制ROS和代谢重编程。PINK1和FOXO3a已被证明在非癌细胞中协同工作。此外,在我们的研究中过表达线粒体超氧化物歧化酶2可以拯救PINK1缺失引起的几种表型。
并非所有细胞类型对PINK1缺失的反应方式都相同。PINK1缺失导致不同细胞类型和背景下产生不同的反应。PINK1表达在神经元和几种其他细胞类型中的缺失已被证明可诱导细胞死亡。我们观察到PINK1下调增加了细胞增殖,这种差异可能归因于我们未能完全消除PINK1表达并维持了促生长的ROS阈值。
ROS在癌细胞中既有促生长也有抗生长作用。尽管我们报告通过PINK1缺失激活ROS在星形胶质细胞中作为促生长信号反应,但可以想象增加的ROS可能对癌细胞产生有害影响。这得到了我们的观察的支持,即PINK1缺失在某些胶质母细胞瘤细胞中导致过度的ROS生成和细胞死亡。此外,在我们的筛选中PINK1的鉴定是在具有活化Ras的星形胶质细胞中进行的,PINK1和Ras信号在代谢和ROS上的相互作用仍有待阐明。
PINK1位于1p36号染色体,这是几种癌症中反复缺失的热点。我们在DNA、RNA、蛋白水平检测到PINK1缺失,并观察到表达PINK1蛋白的胶质母细胞瘤患者生存更好。我们未检测到拷贝数增加或RNA过表达,这提示PINK1作为癌基因的作用。证据也支持PINK1在卵巢癌和乳腺癌中作为肿瘤抑制基因的作用。
鉴定PINK1底物或利用ROS的治疗化合物可能对治疗胶质母细胞瘤和其他癌症有效。
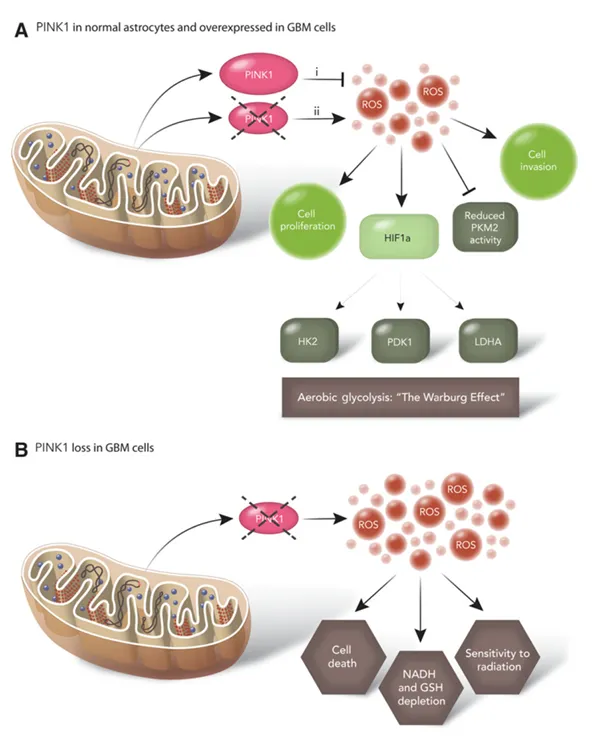
图7:PINK1在胶质瘤中的功能概述。
A、i、PINK1在正常星形胶质细胞中或在重新表达于胶质母细胞瘤细胞中时,能够抑制活性氧(ROS)并抑制有氧糖酵解。ii、正常星形胶质细胞中PINK1的缺失会引发ROS增加,从而稳定HIF水平并促进Warburg效应/有氧糖酵解。
B、胶质母细胞瘤细胞中PINK1的缺失导致ROS水平显着升高,引发氧化应激,进而引发细胞死亡、抗氧化分子耗竭,并使细胞对辐射更加敏感。
- 文章标题:【INC国际大咖研究成果】表达PINK1蛋白的胶质母细胞瘤患者生存结局更好(下)
- 更新时间:2026-05-10 08:26:24

 400-029-0925
400-029-0925