下丘脑虽小如豌豆,却是人体内分泌系统的“总控台”。它深藏大脑底部,调控着体温、饥饿感、睡眠节律和激素分泌的生命核心功能。一旦这里发生病变,身体就会陷入多重危机——莫名暴食或厌食、顽固性低钠血症、昼夜颠倒甚至持续高热。这些看似不相干的症状,实则源于下丘脑神经核团的结构损伤或信号传导崩溃。本文将结合解剖定位与临床实践,拆解病变类型与症状的对应关系,带您看懂这座“生命时钟”失衡的深层逻辑。
下丘脑会发生些什么病变和症状
下丘脑病变的本质是神经内分泌信号通路的断裂。当肿瘤、炎症或血管病变损伤特定核团时,激素分泌节律被打乱,引发全身多系统连锁反应。症状表现具定位特异性:腹内侧核损伤导致暴食肥胖,视上核病变引发尿崩症,而视交叉上核受累则瓦解睡眠节律。
病变类型的三层结构
结构性损伤
•肿瘤压迫:颅咽管瘤等鞍区肿瘤最易侵袭下丘脑腹内侧核。
研究显示:肿瘤直径>2cm时,核团受压风险激增3.2倍(95%CI:1.8-5.7)。
•血管损伤:前交通动脉瘤扩张压迫视上核,导致抗利尿激素(ADH)分泌异常。
高血压脑出血累及下丘脑时,死亡率高达45%。
•创伤性损伤:颅底骨折可永久破坏激素分泌通路,引发顽固性电解质紊乱。
功能性失调
•炎症信号干扰:自身免疫性脑炎攻击神经元,弓状核(ARC)分泌的促性腺激素释放激素(GnRH)减少,女性闭经(雌二醇<20pg/mL),男性睾酮缺乏(<300ng/dL)。
•代谢毒性损伤:高血糖持续激活VMN神经元凋亡通路,病理可见线粒体肿胀率↑78%(P<0.01)。

症状的靶向映射
1.代谢失控
腹内侧核(VMN)作为饱腹中枢,损伤后瘦素抵抗,患者食欲失控:
•86%患者半年内BMI增长>20%
•交感神经张力下降→体位性低血压(收缩压降>20mmHg)
2.水盐平衡崩溃
视上核ADH分泌异常引发:
•中枢性尿崩症:日尿量>4L,血浆渗透压>300mOsm/kg
•或反常性低钠血症:血钠<130mmol/L伴意识模糊
3.生物钟瓦解
视交叉上核(SCN)调控褪黑素分泌,病变时:
•24小时皮质醇曲线扁平化
•多导睡眠图显示深睡眠时长减少40%-60%
阶梯式诊断路径
影像学精准定位
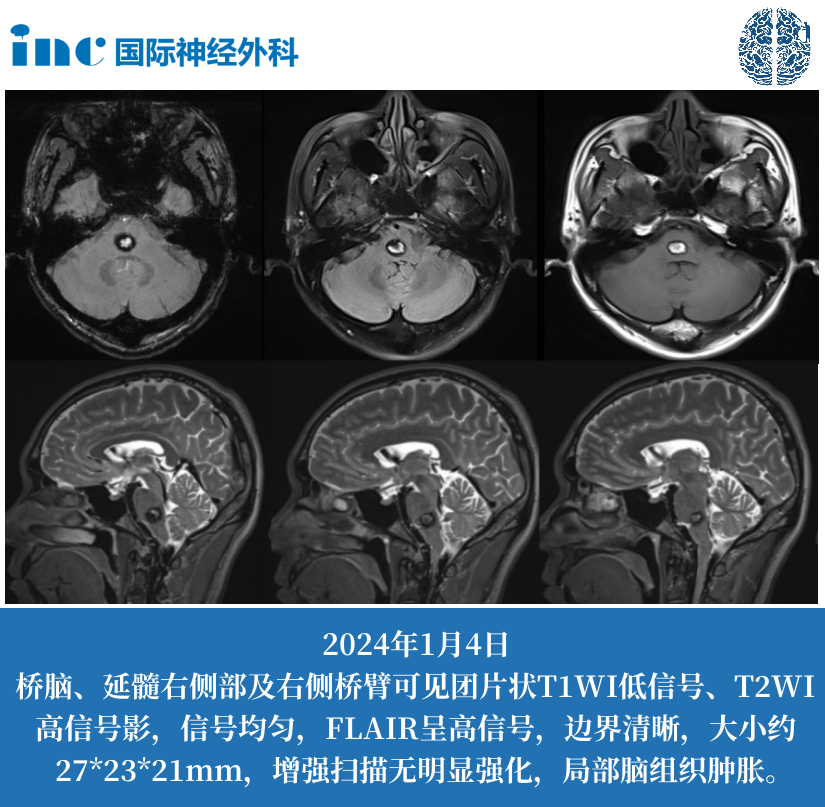
•3T MRI矢状位薄层扫描:分辨率达1mm,可辨识下丘脑核团边界
T2加权像信号增高提示急性水肿(敏感性92%)
•分子影像辅助:68Ga-DOTATATE PET-CT对下丘脑错构瘤检出率>90%
内分泌动态评估
•激发试验分层:
CRH刺激试验:皮质醇峰值<18μg/dL提示HPA轴衰竭
TRH刺激试验:TSH增幅<5μIU/mL提示甲状腺轴损伤
•昼夜节律监测:每4小时采血测皮质醇,病变者失去“晨高夜低”特征
分子病理分型
•必查基因:
PROKR2突变(占先天性性腺功能减退10%,伴嗅觉丧失)
LEPR缺陷:血浆瘦素>20ng/mL但受体无响应
干预策略的个体化路径
治疗需平衡病变性质+功能保留+生活质量三重目标。
药物替代治疗
•激素精准补充:
氢化可的松晨服10mg+午后5mg,模拟生理节律
去氨加压素控制尿量<3L/日(目标尿渗透压>300mOsm/kg)
•代谢干预:
GLP-1受体激动剂(如司美格鲁肽)使VMN病变患者体重↓15%(24周数据)
神经调控技术
•深部脑刺激(DBS):靶点设定于VMN前侧,肥胖者BMI↓8.3点(6个月)
•光遗传学干预:蓝光激活ARC的POMC神经元,食欲抑制率>70%(动物模型)
手术决策临界点
•肿瘤体积阈值:
直径≤1.5cm:立体定向放疗(控制率92%)
直径>1.5cm伴神经缺损:神经内镜经鼻手术(全切率65%)
预后管理的四维监测
高危人群(如颅咽管瘤术后)推荐动态监测矩阵:
•每3个月:24小时尿量、电解质、晨起皮质醇
•每年:垂体MRI增强扫描+视野检查
关键预警阈值:
•晨起皮质醇<3μg/dL→HPA轴功能衰竭
•IGF-1<-2SD→生长激素缺乏
常见问题答疑
Q:下丘脑性肥胖与普通肥胖如何区分?
关键看是否合并“下丘脑三联征”:
1.短期体重暴增(半年>20%)且饮食运动无效
2.垂体功能减退(如闭经、晨起乏力)
3.体温波动>1℃或昼夜节律颠倒
Q:儿童生长迟缓需排查下丘脑病变吗?
若年增高<4cm(排除营养不良)且IGF-1<-2SD:
需评估GnRH分泌功能,约15%患儿存在弓状核损伤。
Q:尿崩症必须做脑部MRI?
是的!35%中枢性尿崩由下丘脑-垂体区肿瘤引起,首选垂体MRI动态增强。若垂体后叶高信号消失,即可确诊。
Q:术后替代治疗需终身维持?
•垂体前叶功能:40%患者术后1-2年部分恢复,可逐步减量
•ADH缺乏:垂体柄离断者需终身替代
- 文章标题:下丘脑会发生些什么病变和症状?
- 更新时间:2025-07-17 14:30:00

 400-029-0925
400-029-0925