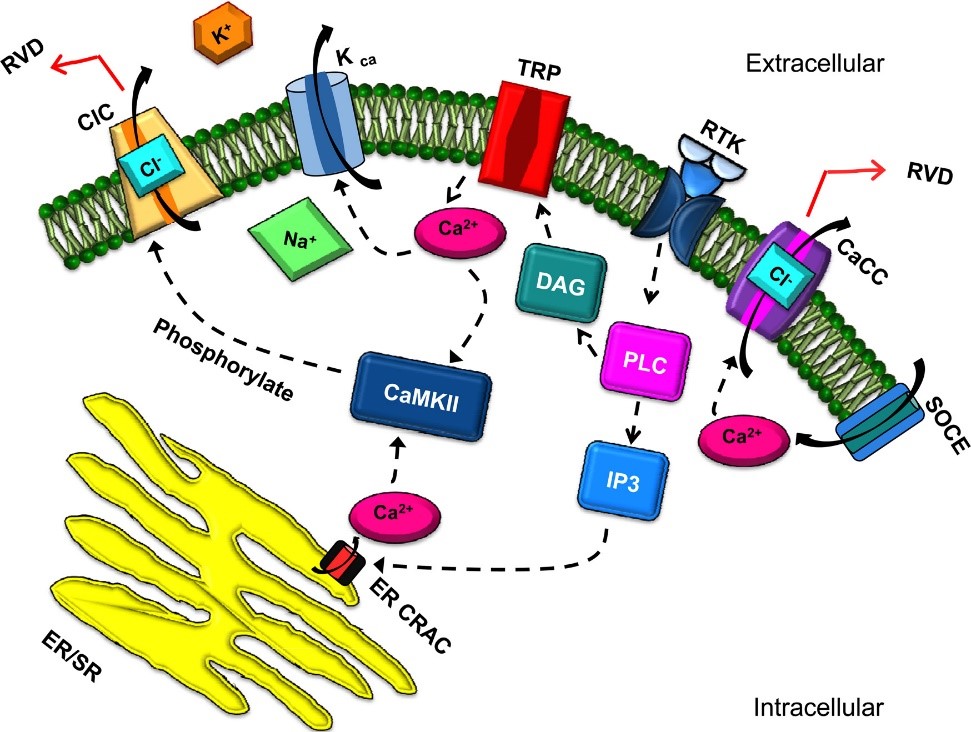
英文摘要:There is tight interplay between Ca2+and Cl−flux that can influence brain tumor proliferation,migration and invasion.Glioma is the predominant malignant primary brain tumor,accounting for 80%of all cases.Voltage gated Cl−channel family(ClC)proteins and Cl−intracellular channel(CLIC)proteins are drastically overexpressed in glioma,and are associated with enhanced cell proliferation,migration and invasion.Ca2+also plays fundamental roles in the phenomenon.Ca2+-activated Cl−channels(CaCC)such as TMEM16A and bestrophin-1 are involved in glioma formation and assist Ca2+movement from intracellular stores to the plasma membrane.Additionally,the transient receptor protein(TRP)channel TRPC1 can induce activation of ClC-3 by increasing intracellular Ca2+concentrations and activating Ca2+/calmodulin-dependent protein kinase II(CaMKII).Therefore,Ca2+and Cl−currents can concurrently mediate brain tumor cellular functions.Glioma also expresses volume regulated anion channels(VRACs),which are responsible for the swelling-induced Cl−current,ICl,swell.This current enables glioma cells to perform regulatory volume decrease(RVD)as a survivability mechanism in response to hypoxic conditions within the tumor microenvironment.RVD can also be exploited by glioma for invasion and migration.Effective treatment for glioma is challenging,which can be in part due to prolonged chemotherapy leading to mutations in genes associated with multi-drug resistances(MRP1,Bcl-2,and ABC family).Thus,a potential therapeutic strategy for treatment of glioma can be through the inhibition of selected Cl−channels.
中文摘要:Ca2+和Cl−电流之间存在紧密的相互作用,可影响脑肿瘤的扩散,转移和侵入。脑胶质瘤是主要的恶性原发性脑肿瘤,占全部病例约80%。电压门控的Cl−蛋白和Cl−细胞内蛋白在神经胶质瘤中急剧过量,并与细胞增长,转移和侵入有关。Ca2+在该现象中也起着重要作用。由Ca2+激活的Cl−(CaCC),如TMEM16A和Bestrophin-1也参与神经胶质瘤的形成,并协助Ca2+从细胞内由存储向质膜移动。此外,瞬时受体蛋白(TRP)通道TRPC1可以通过增加细胞内Ca2+浓度和激活Ca2++钙调蛋白依赖性蛋白激酶II来诱导ClC-3的激活。因此,Ca2+和Cl−电流可以同时调节脑肿瘤细胞的功能。胶质瘤还体现了体积调节的阴离子通道(VRAC),以及导致肿胀的Cl−电流。该电流使神经胶质瘤的细胞能够响应肿瘤在微环境中的低氧状况,从而调节体积减少(RVD)作为生存机制。胶质瘤也可以利用RVD进行侵入和转移。合适治疗神经胶质瘤具有挑战性,部分原因可能是长期化疗与多种药物耐药性相关的基因突变导致。因此,治疗神经胶质瘤的潜在治疗策略可以通过控制特定的Cl−通道。

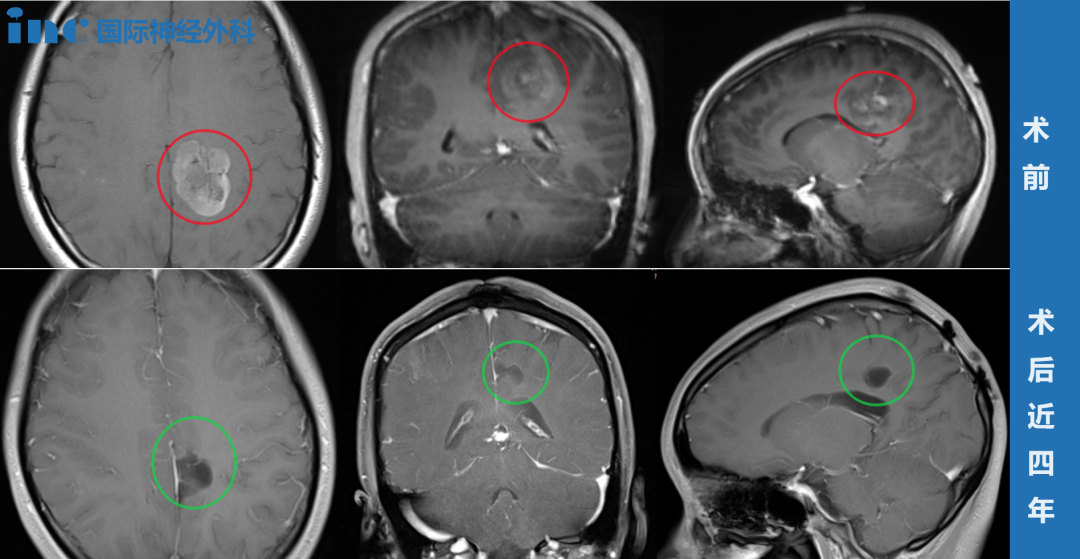
(原发性脑肿瘤有120种,分为良性和恶性肿瘤。分类基于恶性程度,位置和起源的细胞类型。由神经胶质细胞引起的神经胶质瘤代表主要的恶性原发性脑肿瘤。)
2016年,国际卫生组织根据诊断性测试和治疗过程对脑胶质瘤进行了分类修正。目前,神经胶质瘤分为四个等级的恶性肿瘤:低等级(I-II级)和高等级(III-IV级)。这些等级包括星形细胞瘤,少突胶质细胞瘤和室管膜瘤。在高级神经胶质瘤中,间变性星形细胞瘤(III级)占25%,胶质母细胞瘤(GBM)(IV级)占75%。胶质母细胞瘤在扩散,转移和侵入方面格外激进。尽管胶质母细胞瘤表现各不相同,但形态学特征如坏死和血管缺陷使诊断更加可靠。通过分析基因突变和生物标志物可以进一步好转组织学诊断。然而,GBM对常规癌症治疗具有高度的适应力,是一种典型的绝症。即使治疗,患者的预期寿命也很短(约1.5年)。因此,迫切需要新的药物靶点来治疗胶质母细胞瘤。
结论:Cl−通道在神经胶质瘤病理中起重要作用。Cl−流量的调节对于神经胶质瘤的扩散,转移和侵入至关重要。当有异常情况时,Cl−通道可以控制胶质细胞凋亡并提高生存能力。
考虑神经胶质瘤的治疗时,有两个主要类别的Cl−通道需要进一步检查:1)在产生肿胀的Cl−电流中起作用的通道,以及2)直接影响细胞扩散和生长的。氯电流在调节细胞体积,特别是调节体积减少(RVD)中起着关键作用,RVD可以维持细胞活力,促进细胞的侵入和转移并启动扩散信号通道。氯电流很可能是由ClC-3在神经胶质瘤中产生的,它代表了潜在的治疗靶标。其他潜在药物靶标包括CLIC1和TMEM16A,它们是Cl−通道,并可以直接影响神经胶质瘤细胞的扩散和生长。此外,在文献中有强有力的证据支持Cl−和Ca2+信号传导之间的重要关系,有助于肿瘤恶性发展。靶向Cl−通道的治疗药物可以利用Cl−和Ca2+的相互作用,并且可能是胶质瘤治疗的关键。

关于加拿大James T.Rutka教授
在国际神经外科的癫痫治疗领域,有这样一位国际盛名的癫痫/脑瘤咨询专家(擅长小儿神经外科相关疾病),他曾任美国神经外科学会、美国神经外科医师协会会员,目前在担任国际神经外科杂志《Journal of Neurosurgery》主编,现在同时也是INC世界神经外科顾问团的教授。他就是鼎鼎大名的加拿大James T.Rutka教授。

James T.Rutka教授曾与名古屋大学的杉田健一郎(Kenichiro Sugita)博士在微血管神经外科领域开展了临床研究,并于1990年在东京骏天大学(Juntendo University)获得了分子免疫学博士后研究奖学金。教授发表了超过500多篇的文章,在临床上的研究方向以颅内肿瘤为主,对胶质瘤、纤维瘤、颅咽管瘤、室管膜瘤具有多年的临床经验,擅长清醒开颅术及显微手术。在最近的临床研究上,教授又将重点集中在了儿童脑瘤和癫痫的外科治疗上,并取得了合适的成果。
其实验室在研究脑肿瘤生长和侵袭的机制方面颇有成就,并在Sunnybrook健康科学中心和多伦多大学生物材料和生物医学工程研究所的合作下,正在设计一种基于纳米颗粒的输送系统,作为治疗胶质瘤的一种新方法。
原文链接:http://npub.ltlogo.top/31129471/
- 文章标题:加拿大James Rutka教授:Cl-通道在原发性脑肿瘤中的作用
- 更新时间:2020-07-03 11:46:52

 400-029-0925
400-029-0925