表皮生长因子受体三型突变EGFRVIII则使酪氨酸残基磷酸化,产生鸟嘌呤核苷酸的细胞交换因子,因而造成EGFRvⅢGBM细胞生长。其中ABT-414是合适微管控制剂(单甲基阿里他汀F...
2012 年中国肿瘤登记报告指出,中国脑及中枢神经系统恶性肿瘤病死率为3. 87 / 10 万,其中,
胶质瘤占中枢神经系统CNS恶性肿瘤81% 。 脑胶质瘤严重危害人的健康,目前的治疗仍是以手术治疗为首要 原则 ,术后辅助放化疗,然后肿瘤的高度恶性使得预后很差,。 随着分子肿瘤学研究的发展,2016 年5 月,国际卫生组织WHO发布四版(修订)的CNS肿瘤分类,一次推出整合了组织学表型和基因表型的CNS肿瘤分类。 根据WHO的CNS肿瘤新分类和当前的研究热点,本文对脑胶质瘤分子基因检查及 分子靶向药物治疗胶质瘤进行详细解读。
胶质瘤分子标志物解读
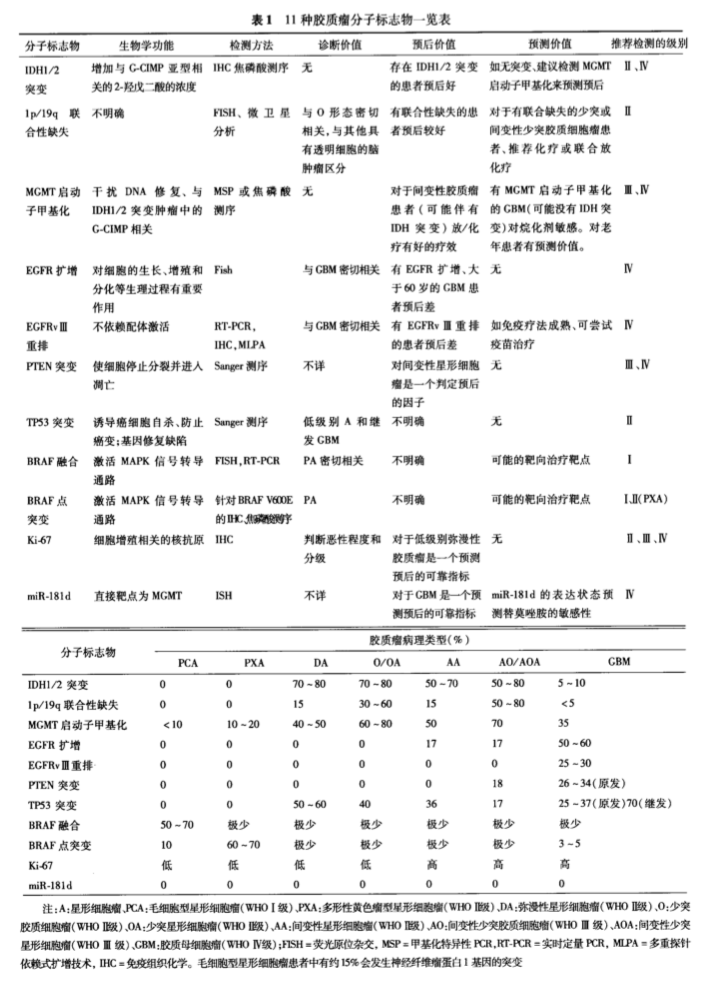
近年来,神经肿瘤分子病理取得了进展,目前已发 现一系列有助于脑胶质瘤临床诊断和预后判断的分子标志物。 目前的WHO病理分级仍然依赖形态学进行肿瘤分级,然而,有 充分的证据表明,组织特征相同或相似的胶质瘤可以具有不同的分子遗传学背景,导致WHO分级相同的个体间预后有着较大差异。基于肿瘤遗传学水平的分子病理分型能够更准确地判断 临床预后;并且对组织学上较难鉴别的混合性胶质瘤(少突星形 细胞瘤和间变性少突星形细胞瘤)还能帮助明确诊断和分级。 另外,这些新近发现的分子变异有可能成为未来治疗的新靶点。
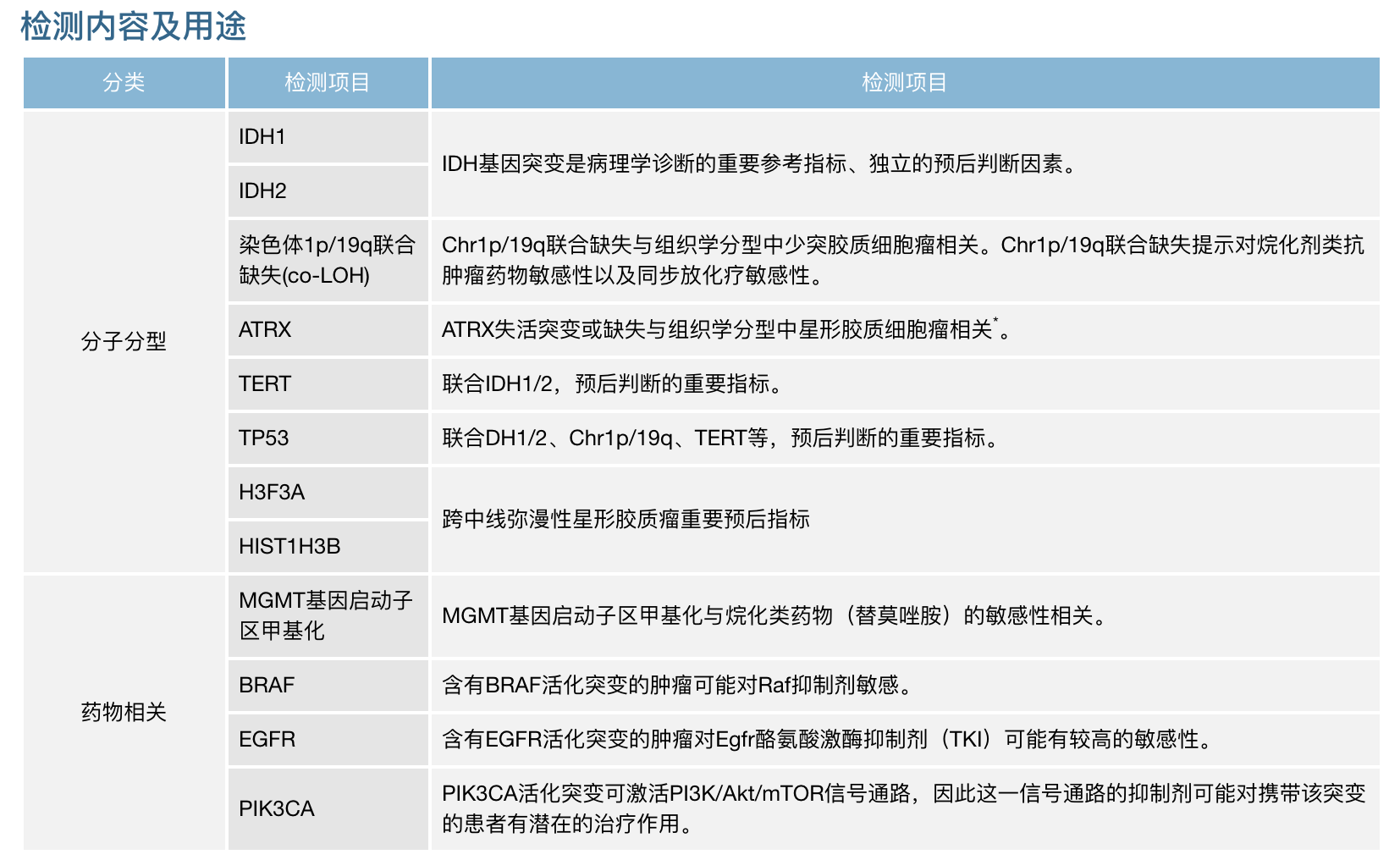
(图:11种胶质瘤分子标记物一览)
(图:胶质瘤常用检测分子 及意义总结)
近10年来,脑胶质瘤的基础和临床研究有了较大突破,进一步了解胶 质瘤的分子生物学特征,通过l临床试验明确更多潜在的分子标 志物,有望揭开脑胶质瘤病理生理和发病机制的神秘面纱。除 了种族、性别、年龄、生活习惯等临床常见因素,重要的分子标志 物的筛选,对临床胶质瘤 进一步病理分型的诊断、治疗 及预后判断等均有深远的意义。
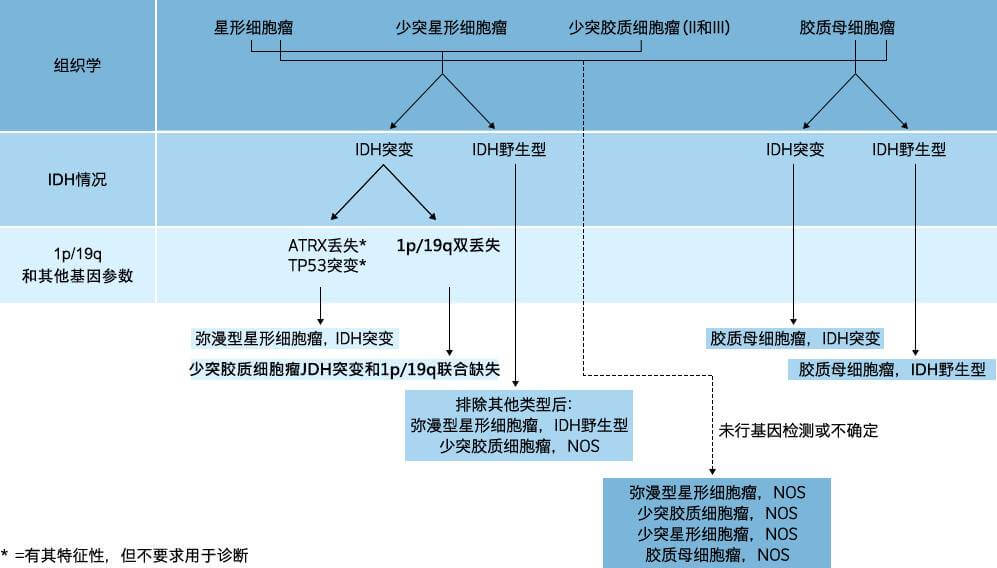
图:胶质瘤分子基因诊断图示
参考资料:
中国脑胶质瘤分子咨询指南.
分子靶向药物治疗脑胶质瘤的研究进展.
- 文章标题:胶质瘤基因检测解读及分子靶向药物治疗进展
- 更新时间:2023-03-26 19:54:26
-
胶质瘤是需要放化疗,但如果是一级胶质瘤,不需放化疗。假如一级胶质瘤没有切除完全...
2022-05-31 11:13:07
-
脑胶质瘤四级一般预后较差,5年生存率较低,这些预后因素影响着脑胶质瘤四级能活多...
2021-02-04 11:13:22
-
神经胶质瘤是成人中常见的原发性恶性脑肿瘤。它们可以发生在中枢神经系统中的任何位...
2020-12-07 16:30:22
-
偶然发现的胶质瘤需要手术吗?一般情况下患有胶质瘤病人一经发现尽早手术,推迟手术...
2021-03-02 14:55:02
-
各种临床研究证明,面对胶质瘤、脑膜瘤、颅咽管瘤、脊索瘤等部分恶性脑肿瘤,硼中子...
2020-07-07 13:33:13
-
岛叶胶质瘤手术要多少钱?能报销吗?岛叶靠近大脑中动脉和透镜状动脉、原发运动区和...
2023-11-07 18:07:53
-
一级别胶质瘤是癌症吗?癌症是可以影响身体任何部位的一大类疾病的统称。一级别胶质...
2021-08-03 11:25:15
-
左侧基底节区胶质瘤能活多久?需手术吗?左侧基底节区胶质瘤的预后与多个因素有关,...
2023-11-13 15:08:44
-
胶质瘤手术应根据影像学、术中导航和电生理检测来判断切除范围,在保留神经功能的前...
2022-05-31 10:20:31
-
儿童高级别脑胶质瘤的传统治疗方式为手术切除,术后再行放化疗,如今,靶向治疗逐渐...
2021-01-07 16:48:58
-
枕叶胶质瘤的优选治疗方法是手术。左枕叶通常没有重要的功能区域。手术是较好的选择...
2022-05-31 11:02:24
-
作为一种较为常见的原发性颅内肿瘤,脑胶质瘤是指起源于脑神经胶质细胞的肿瘤。国际...
2020-06-09 14:46:20
-
病史:2020年8月底,患者因单位体检颅脑磁共振平扫发现右脑异常信号。 2020年9月初,检查...
2023-04-05 20:17:48
-
松果体胶质瘤症状?松果体胶质瘤起源于松果体区域的胶质细胞。它通常会对人体的神经...
2023-11-11 14:06:32
-
大多数视神经胶质瘤生长缓慢且无癌性(良性)。肿瘤的缓慢和自限性生长表明,在大多...
2021-02-22 13:39:35
-
基因检测是指通过特定设备对被检测者细胞中的DNA分子信息作检测,分析其所含有的基因...
2022-07-05 16:29:25
-
原本是二级的少突胶质细胞瘤,为什么一年多就发展到了4级?临床上这样的案例多见,...
2022-06-01 13:50:21
-
胶质瘤不会遗传。目前没有证据表明胶质瘤是遗传性的。胶质瘤的发生与基因和环境有关...
2019-06-01 11:02:00
-
目前对于低级别脑胶质瘤的化疗还存在争议,主要包括:化疗的时机、化疗方案的选择、...
2021-03-04 15:46:49
-
胶质母细胞瘤(GBM)是成人原发性恶性脑肿瘤中常见和具侵袭性的。目前,一线治疗包括...
2023-03-26 20:12:01

 400-029-0925
400-029-0925