毛细胞星形细胞瘤约占全部儿童脑肿瘤的25%。它在生命的前20年发展,较常见的位置是小脑和下丘脑/视神经。在磁共振成像中,毛细胞星形细胞瘤通常是一种界限清楚的病变,通常具有囊性和结节状成分,可不均一地增强对比度。在组织学上,它有一个特征性的模式,密集的纤维区域散布着微囊(双相模式)。罗森塔尔纤维经常遇到,是一个有用的病理标志。标准的初始方法是手术切除。然而,完全手术切除并不总是可行的。化疗作为辅助疗法,优于不能好转预后且具有较高认知和内分泌影响的长期发病率的放疗。这些患者预后良好,即使肿瘤切除不完全,10年生存率也高达80%。有时会出现不利的演变,如恶性转化、局部复发、多中心疾病或软脑膜扩散。恶性转化发生在不到5%的病例中,在以前接受过放疗的患者中更为常见。下文描述了一个小脑毛细胞星形细胞瘤在12年没有放疗后自发恶性转化的病例。
病史摘要
一名15岁的男孩较初在3岁时被送到医院。他是父母的三个孩子。没有已知的神经、肿瘤或遗传疾病家族史。他以前的个人历史并不引人注目。3岁时,他被电脑断层扫描诊断为右侧小脑半球的囊性肿瘤,并接受了完整的手术切除。组织学检查证实了与毛细胞星形细胞瘤诊断一致的发现。虽然观察到轻微的核多态性和轻微的内皮细胞增殖,但没有坏死、有丝分裂和微血管增殖,Ki-67增殖指数低,p53免疫染色阴性(核染色阳性的癌细胞不到10%)。
未给予辅助治疗。手术后,临床和图像监测没有显示复发的证据。他在10岁时失访。5年后,患者出现间歇性头痛和呕吐3个月的病史。在诊断的时候,他出现了意识改变,共济失调和节奏障碍。电脑断层扫描显示在右脑半球有一个大的囊性病变并有出血成分。肿块增强了造影效果,导致梗阻性脑积水(图2A和B)。
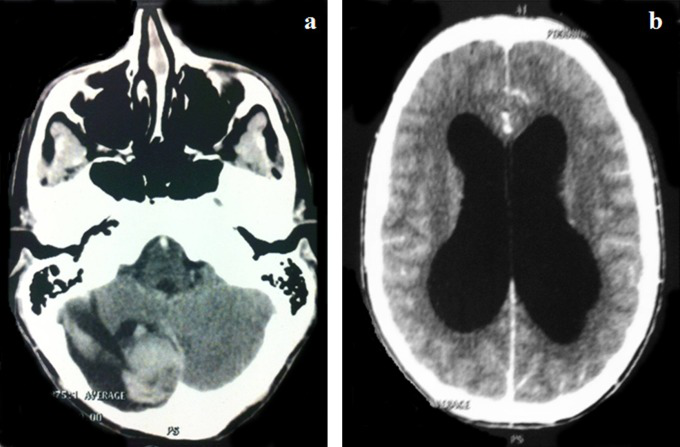
图1:轴位扫描后计算机断层扫描显示局部复发,毛细胞星形细胞瘤诊断后12年。带有出血成分的右侧囊性小脑肿瘤。病变引起的脑积水。
病人接受了二次手术,病灶全部切除。手术及术后期间均顺利进行,二次手术后的磁共振成像未显示任何残留病变或髓质病变的迹象。与病理对照,12年前的组织病理结果与胶质母细胞瘤一致,显示间变性和多形性细胞,坏死,内皮细胞增生,Ki-67免疫染色高增殖指数,p53阳性。
二个病灶的比较基因组杂交分析见表1。BRAF基因15外显子突变在1例和2例肿瘤中均未发现。他接受了高剂量甲氨蝶呤、顺铂、依托泊苷、异环环胺和长春新碱的辅助治疗,外加局部放疗(59.4 Gy)。治疗结束两个月后,磁共振成像显示背侧软脑膜播散(图2)。
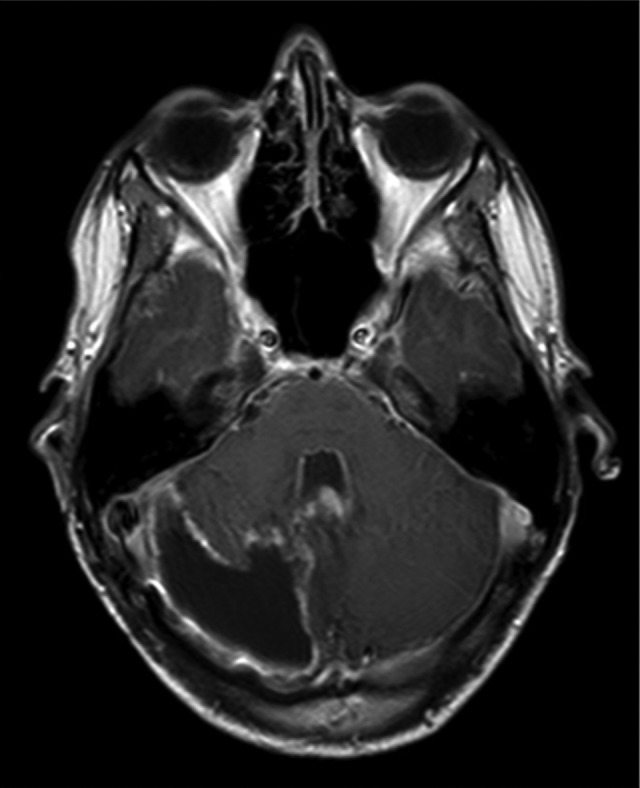
图2:辅助治疗后轴位T1加权磁共振成像显示异常软脑膜对比增强。
患者随后接受5个疗程的替莫唑胺治疗,并对症状性背侧病变进行局部放疗。5疗程替莫唑胺后2个月,患者出现神经功能迅速恶化。神经影像学显示进行性的颅内和脊髓软脑膜播散和脑室系统出血。在诊断为胶质母细胞瘤后16个月和毛细胞星形细胞瘤后14年因疾病进展而死亡。
案例分析
该病例说明了低度恶性胶质瘤演变为恶性胶质瘤的潜在风险。其潜在机制尚不清楚。在大多数已发表的病例报告中,患者曾接受过放疗。因此,这种疗法被认为是恶性变化的一个关键因素,尽管没有关于累积发病率、危险因素和分子异常的可用信息。以前没有放疗的恶性转化也有报道,但偶尔发生在儿童时期和小脑以外的部位。
一直与肿瘤复发或恶性变性相关的因素是术前造影增强成像,通常提示为高级别胶质瘤,但也可能出现在15%至40%的低级别胶质瘤患者中;肿瘤大小,因为肿瘤大小每增加1厘米,复发风险增加1.3倍;和分子异常。
一旦对比增强程度被用作恶性肿瘤的指标,磁共振成像是在胶质瘤自然史的早期检测胶质瘤的重要诊断工具,并且缺乏对比增强可能提示低度恶性胶质瘤。然而,一些非增强性病变可能是恶性的。因此,放射特征是用于评估治疗反应和结果的标准组合的一个组成部分。其他标准包括临床发现(患者年龄、神经功能状态和肿瘤位置)、手术切除程度、组织学特征、增殖指数和分子特征。
关于低级别胶质瘤的分子特征,鉴定了许多数量和结构异常,其中染色体7、8和17是较常受影响的。然而,传统的染色体组型分析在多项研究中未被揭示,7号染色体是一致的发现。17p (p53位点)的缺失与疾病的快速复发有关,因为p53调节细胞周期停滞、DNA修复、凋亡、自噬、衰老、多能性控制和干细胞自我更新的控制。p53肿瘤控制基因在胶质瘤形成的早期阶段经常突变或缺失。一种假设是,由于位于受保护小生境区域的神经干细胞的恶性转化,高级别胶质瘤可能会出现和复发。儿童的TP53突变仅限于经历恶性转化的低级胶质瘤的5%至10%。最近,多组报道在7q34区域有一个小的非随机重复,包含一个BRAF-基亚1549基因融合。该基因存在于60%至80%的散发性毛细胞星形细胞瘤患者中,并与幕上定位、复发和不完全切除相关。
本案例报告比较特别,原因如下。首先,这是一开始描述儿童小脑低级别胶质瘤的自发恶性转化。二,p53在继发性肿瘤中表达,而在原发性肿瘤中不表达,这证实了p53在转化过程中的作用。毛细胞型星形细胞瘤的比较基因组杂交分析显示了这种类型肿瘤的较一致的发现,即7号染色体的增加。没有发现之前描述的其他分子异常。由于低级别胶质瘤的特征似乎与分子和细胞生物学特征密切相关,因此需要对大量患有低级别胶质瘤恶性转化的儿童进行临床、分子和预后分析,以阐明其病理生理机制。
总之,对诊断为低级别胶质瘤的患者进行长期随访的必要性。分子和生物变异可能存在,因此需要进一步的基因型研究,以评估哪些低级别胶质瘤将进展为高级别胶质瘤,并可受益于更的辅助治疗。
毛细胞星形细胞瘤案例相关报道
阅读:3例成人脑干胶质瘤全切手术剖析,术后超过5年以上均未复发
- 文章标题:低级别胶质瘤会恶化吗?毛细胞星形细胞瘤恶化案例一则
- 更新时间:2021-01-15 16:03:50

 400-029-0925
400-029-0925